Kingdom Fungi (Jamur)
Fungi ( Jamur )
Kali ini saya akan membahas tentang fungi ( jamur ) dimana jamur merupakan kingdom tersendiri dari system taksonomi. Beberapa jamur ada yang mendatangkan keuntungan bagi manusia sebagai sumber lemak dan glikogen atau sebagai pengurai pada suatu lingkungan ekosistem.
A. Ciri – Ciri Jamur
Adapun ciri – ciri jamur sebagai berikut.
- Tubuh jamur bersel banyak, dinding selnya tersusun atas zat kitin, mempunyai membran inti (eukariotik) akan tetapi tidak dapat membuat makanannya sendiri.
- Jamur bersel banyak (multiseluler) yang terdiri atas benang – benang halus yang disebut dengan hifa.
- Cabang dari hifa disebut dengan miselium yang berfungsi menyerap makanan dari substratnya.
- Bersifat saprofit dan parasit
- Berkembang biak dengan cara aseksual dengan konidium yang dilakukan oleh jamur bersel tunggal (uniseluer) yaitu dengan pertunasan atau dengan cara pemutusan hifa (fragmentasi).
- Perkembang biakan secara seksual dilakukan dengan membentuk askus spora didalam basidium. Beberapa perkembangan seksual pada jamur antara lain anisogami, isogami, oogami, gametangiogami dan somatogami.
- Beberapa jenis jamur dapat membentuk alat perlindungan diri dari suatu lingkungan yang buruk antara lain teletospora, klamidospora, dan gemma. Kadang kala alat tersebut berupa kumpulan benang miselium yang bentuk badan seperti umbi, disebut dengan sklerotium.
B. Klasifikasi Jamur
Dunia fungi dibedakan menjadi 4 devisi, yaitu zygomycotina, Ascomycotina, Basidiomycotina dan deuteromycotina. Devisi pada jamur akan saya jelaskan satu persatu akan tetapi sebelumnya perhatikan table dibawah ini dahulu.
|
No |
Divisi |
Contoh |
Nutrisi |
Keterangan |
| 1 | Zygomycotina | Jamur hitam, roti,Rhizopus stolonifer,Mucus hiemalis,Metarsium anisopliae, dan Beauveria bassiana | Saprofit, beberapa jenis simbiosis dan beberapa jenis parasit | Reproduksi seksual dengan zigospora, reproduksi aseksual dengan spora yang tumbuh dari hifa,beberapa jenis berasosiasi dengan akar tanaman. |
| 2 | Ascomycotina | Jamur roti pink, ragi, morel,Saccharomyces cerevisiae, penicillium notatum, dan Neourospora crassa | Saprofit dan beberapa jenis parasit | Reproduksi secara aseksual melalui konidia pada konidiofora. Reproduksi secara seksual dengan askospora pada askus. Merupakan divisi terbesar yang bersimbiosis dengan alga dan alga membentuk likenes. |
| 3 | Basidiomycotina | Jamur merang, jamur kuping,Volvariella volvaceae, Amanita phalloides, Genoderma aplantum dan Puccina gaminis | Hara tanah dan menghancurkan tanaman | Reproduksi seksual melalui basidiospora, sebagian dapat dimakan dan ada yang bersifat sebagai racun yang mematikan. |
| 4 | Deuteromycotina | Helminthosporium oryzae, Tinie versicolor, Epidermophyton floocossum dan Fusarium | Saprofit dan parasit | Fase seksual dengan konidia yang belum jelas diketahui tahapan seksualnya. |
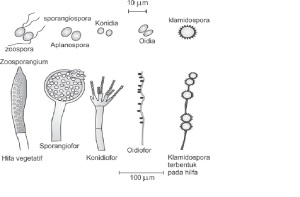
Divisi Zygomycotina
Nama zygomycota berasal dari jenis perbanyakan diri seksual, terutama pada pembentukan zigospora. Jamur divisi ini biasanya hidup di darat sebagai saprofit, dinding selnya tersusun atas zat kitin dan soenositik dimana tidak mempunyai zoospore sehingga sporanya merupakan sel- sel yang berdinding dan mempunyai haustoria. Spora inilah yang akan tersebar kemana – mana, tubuhnya berupa hifa tidak bersekat dan mempunyai miselium bercabang banyak.
Perkembang biakannya secara aseksual dengan sporangium yang menghasilkan spora sedangkan perkembangbiakan seksualnya dengan gametangiogami dengan cara peleburan dua hifa yaitu hifa betina dan hifa jantan. (gametangium yang sama bentuknya dan memiliki banyak inti mengadakan kopulasi yang menghasilkan zigospora).
Kelompok kelas ini memiliki tiga jenis hifa, yaitu hifa yang menjalar dipermukaan substrat disebut stolon, hifa yang menembus ke dalam substrat seperti akar disebut rizoid, dan hifa yang menjulang ke atas dan membentuk sporangium disebut sporangiosfor.
Daur hidup Zygomycotina sebagai berikut akan saya jabarkan :
- Hifa (+) dan hifa (-) akan saling berdekatan
- Pada masing – masing hifa yang berdekatan membentuk cabang hifa. Diujung hifa tadi akan tumbuh bakal gametangium.
- Bakal gametangium berubah menjadi gametangium dan mempunyai banyak inti.
- Dinding gametangium akan pecah, inti (+) dan inti (-) bergabung menghasilkan zigospora yang berisi inti – inti diploid atau 2n. Diantara inti – inti diploid yang terbentuk hanya satu yang hidup, sedangkan yang lain akan mengalami degenerasi.
- Selanjutnya zigospora akan tumbuh, dindingnya menebal, tampak berwarna hitam dan banyak mengandung bahan makanan cadangan . Selanjutnya zigospora mengalami fase istirahat yang cukup lama.
- Jika kondisi lingkungan sesuai zigospora akan tumbuh. Sporangium yang terbentuk ditopang oleh hifa penunjang yang disebut dengan sporangiofor. Inti haploid akan membelah secara mitosis menjadi inti – inti spora yang terdapat di dalam sporangium. Spora yang dihasilkan berupa spora (+) dan (-).
- Jika sporangium telah masak dindingnya akan pecah dan sporanya akan tersebar keluar.
- Jika spora jatuh pada substrat yang sesuai akan tumbuh menjadi hifa baru. Spora (+) akan tumbuh menjadi hifa (+) dan spora (-) akan tumbuh menjadi hifa (-).
- Selanjutnya setiap hifa dapat berkembang biak secara aseksual dengan membentuk sporangium pada setiap ujung hifanya. Sporangium dari hifa (+) hanya akan menghasilkan spora (+) dan sporangium dari hifa (-) akan menghasilkan spora (-).
Divisi Ascomycotina
Ascomycotina adalah kelompok jamur yang berkembang biak dengan membentuk spora didalam selnya (kantung kecilnya) yang disebut dengan askus. Pembentukkan askus inilah yang menjadi ciri ascomycotina. Tubuh jamur ini hifanya telah memiliki sekat dan berinti banyak dan spora tidak berflagella. Keanekaragaman divisi ascomycotina adalah yang paling besar dibanding divisi lainnya. Jamur golongan ini hidup sebagai parasit pada organisme lain, saprofit pada sisa organisme, dan ada pula yang hidup bersimbiosis dengan alga biru dan alga hijau bersel satu membentuk linekes .
Alat perkembangbiakan secara seksual berupa askus yang akan menghasilkan askospora. Spora dihasilkan didalam alat yang bebentuk seperti botol, pemebentukkan ini disebut dengan endospora. Beberapa askus berkumpul membentuk tubuh buah yang disebut dengan askoskarp. Sedangkan alat perkembangbiakan aseksual dengan cara spora yang dihasilkan oleh konidium, fragmentasi dan pertunasan. Askus adalah sporangium yang menghasilkan askospora, pembentukkan askospora dilalui oleh beberapa tahapan berikut ini :
- Kopulasi antara gametangium jantan ( anteredium ) dan gametangium betina (askogonium).
- Plasmogami yaitu bersatunya plasma kedua gametangium tersebut.
- Kariogami yaitu persatuan dua inti yang berasal dari dua gametangium tersebut, yang akan menghasilkan zigot inti yang diploid.
- Dari zigot inti dilanjutkan dengan pembentukkan askospora secara endogen melalui pembelahan reduksi.
Daur hidup Ascomycotina akan saya jabarkan sebagai berikut :
- Askospora atau konidiospora akan tumbuh menjadi miselium.
- Satu atau beberapa ujung hifa berdiferensiasi. Ada yang berdiferensiasi menjadi anteridium dan ada yang berdiferensi menjadi arkogenium. Masing – masing gametangium berisi inti haploid. Kedua gametangium ini letaknya berdekatan.
- Terjadi kopulasi antara arkogenium dengan anteredium dengan membentuk saluran penghubung antara arkogenium dan anteredium
- Selanjutnya terjadi plasmogami. Inti anteredium pindah ke arkogenium membentuk zigot inti.
- Zigot ini akan membelah secara reduksi menghasilkan inti yang haploid. Bersamaan dengan itu dari arkogen akan tumbuh hifa – hifa arkogenium. Inti – inti haploid yang tetap berpasangan akan pindah kedalam hifa arkogenium.
- Hifa arkogenium akan bercabang – cabang dan membentuk sekat. Segmen hifa dekat arkogenium mengandung banyak inti sedangkan ujungnya mengandung sepasang inti haploid. Bagian yang mengandung inti haploid inilah yang akan tumbuh menjadi askus.
- Hifa arkogenium beserta miselium vegetative akan tumbuh kompak membentuk askokarp atau badan buah.
- Selanjutnya pasangan inti haploid di dalam arkogenium akan bergabung membentuk inti diploid, inti tersebut membelah secara meiosis menghasilkan empat sampai delapan inti haploid yang dikelilingi oleh selaput. Inilah yang disebut sebagai askospora.
Berikut beberapa contoh ascomycotina yang penting peranannya bagi manusia
- Neurospora
Jamur ini dikenal dengan nama jamur oncom merah, jamur ini tumbuh subur pada oncom dan tongkol jagung rebus yang telah dihilangkan bijinya. Disamping itu sering juga digunakan sebagai objek penelitian genetika yaitu untuk meneliti pengaruh sinar x terhadp peristiwa mutasi, jamur ini banyak juga digunakan untuk membuat oncom.
- Penicilium
Jamur ini tumbuh pada makanan yang mengandung gula seperti roti, nasi dan pada buah yang telah ranum. Pada roti atau buah jamur ini Nampak seperti noda hijau atau kebiruan.
Jamur ini berkembang biak secara aseksual dengan konidium dan secara aseksual dengan askus. Ujung konidiofor penicilium tidak membesar tetapi bercabang – cabang. Dari ujung cabang konidiofor inilah berderetan konidium. Jamur ini berperan penting dalam industry kesehatan dan makanan Strain penicillium notatum dan penicillium chrysogenum mampu menghasilkan antibiotika penisilin .
- Trichoderma
Beberapa species jamur marga Trichoderma mampu menghasilkan enzim selulose, sehingga dapat mencernaan selulosa atau sering bersifat selulotik. Trichoderma reesei adalah salah satu spesies dari marga ini yang menghasilkan enzim selulose yang dapat diisolasikan dengan murni. Selulose dapat digunakan untuk memproduksi protein sel tunggal.
- Aspergillus
Aspergillus hidup berkoloni pada bahan makanan, pakaian, maupun alat rumah tangga lain yang lembab dan kurang sinar matahari. Badan buah berupa kleistostium atau kadang berupa setukal hifa yang tidak beraturan. Askusnya bulat tersebar tidak beraturan dan tersimpan didalam selubung. Sporanya baru dapat tersebar keluar jika selubung buahnya pecah. Aspergillus berkembang biak secara aseksual dengan konidium. Ujung tangkai konidium membesar dan tumbuh sterigma dengan konidium yang berderet di ujung sterigma tersebut. Jenis – jenis aspepergillus yang sering digunakan antara lain adalah : Aspergillus oryzae ( untuk pembentukan sake),Aspergillus wenti ( untuk pembuatan tauco ,asam nitrat, asam formiat, dan asam oksalat), Aspergillus niger(menghilangkan oksigen pada sari buah dan menghasilkan enzim pektinase dan glukosa oksidase).
Divisi Basidiomycotina
Basidiomycotina mempunyai ciri – ciri sebagai hifa bersekat, hifa vegetatifnya mempunyai satu inti yang haploid, mempunyai basidioskarp dan badan buah yang seperti payung, Basidiomycotina merupakan kelompok jamur yang pembentukan sporanya terjadi di atas sel yang di sebut basidium. Jamur kelompok ini berkembang biak secara aseksual dengan membentuk konidium dan berkembang biak secara seksual dengan membentuk spora basidium. Cara hidup jamur ini ada yang saprofit, parasit pada tumbuhan dan ada pula yang bersimbiosis membentuk mikoriza pada akar tumbuhan.
Daur hidup Basidiomycotina sebagai berikut akan saya jabarkan :
- Basidiospora atau konidiospora tumbuh menjadi hifa bersekat dengan satu inti
- Ujung dua hifa yang berbeda starinnya (strain (+) dan strain (-)) bersinggungan dan dinding selnya akan larut. Inti sel dari strain (+) pindah ke strain (-), sehingga dihasilkan dua inti atau dikariotik.
- Sel dikariotik tumbuh menjadi miselium dikariotik.
- Miselium tumbuh menjadi badan buah yang bentuknya sesuai dengan badan buah sebelumnya.
- Hifa – hifa di bagian bawah basidioskarp membentuk basidium. Dua inti pada sel basidium bersatu, sehingga dihasilkan inti diploid (2n)
- Sel basidium membesar, pada ujungnya terbentuk 4 buah tonjolan atau sterigma. Sementara itu intinya yang diploid membelah reduksi , dihasilkan 4 inti haploid.
- Masing – masing inti haploid masuk kedalam tonjolan terbentuklah 4 spora dengan sebuah inti haploid
Beberapa jenis jamur Basidiomycotina dapat dimanfaatkan sebagai sumber makanan. Contohnya Volvariella volvacea, Amanita phalloides, Ganoderma aplantum, Pleurotes dan Puccina graminis.
Divisi Deuteromycotina
Deuteromycotina mempunyai ciri – ciri hifa bersekat dan dinding selnya terbuat dari zat kitin, jamur ini berkembang biak dengan konidia dan belum diketahui tahap seksualnya sehingga jamur ini sering disebut dengan jamur imperfecti yaitu jamur yang belum sempurna. Beberapa jenis jamur yang hingga kini masih dikelompokkan ke dalam devisi Deutromycotina antara lain sebagai berikut :
- Helminthosporium oryzae, hidup sebagai parasit, perusak kecambah dan buah, serta menimbulkan noda – noda pada daun inang. Buah yang terserang menjadi menyerupai bludru.
- Sclerothium rolfosii, menyebabkan penyakit busuk pada tanaman budi daya
- Epidermophyton floccosum penyebab penyakit kaki atlet
- Microsporum, Trichophyton dan Epidermophyton merupakan penyebab penyakit kurap yaitu sejenis penyakit kulit.
Mikoriza
Merupakan jamur yang bersimbiosis dengan akar tanaman dimana tanaman akan mendapatkan keuntungan berupa air dan mineral dan unsur hara yang berguna untuk melakukan proses fotosintesis dan dengan adanya mikoriza maka tingkat penyerapan tumbuhan akan meningkat, sedangkan bagi jamur sendiri akan mendapatkan keuntungan berupa zat organik dari tanaman sebagai nutrisi untuk jamur tersebut.
Jamur yang membentuk mikoriza berasal dari golongan Zygomycotina, Ascomycotina, atau Basidiomycotina. Mikoriza dibedakan menjadi 2 tipe, yaitu:
Ektomikoriza, hifa tidak menembus ke dalam akar (korteks) hanya sampai epidermis, contoh: ektomikoriza pada pinus.
Endomikoriza, hifa jamur menembus akar sampai ke bagian korteks.
Contoh: endomikoriza pada tanaman anggrek dan sayuran seperti kol dan bit.
Untuk lebih jelas bisa diperhatikan gambar dibawah ini sebagai perbedaan Ektomikoriza dan Endomikoriza.
Likenes ( Lumut Kerak )
Likenes atau lumut kerak adalah simbiosis antara alga dengan jenis jamur tertentu. Alganya biasa berasal dari alga hijau dan biru bersel satu, sedangkan jamurnya berasal dari Ascomycotina atau Basidiomycotina. Likenes hidup sebagai epifit pada batang pohon dan hidup pada permukaan bebatuan beberapa jenis hidup pada celah bebatuan yang sering disebut dengan endolitik.
Karena kemampuan likenes mampu membantu pelapukan bebatuan sebagai proses pembentukan tanah, maka likenes terkenal dengan sebutan organisme perintis. Tubuh likenes bertalus, bagian luarnya tampak seperti susunan miselium yang kompak sedangkan pada bagian dalamnya terdapat susunan hifa yang longgar dan diantara hifa yang longgar ini terdapat sel – sel alga.
Cara reproduksi likenes tidak mempunyai perkembangbiakan yang khusus. Dalam lingkungan yang kering jalinan hifa – hifa jamur-alga dapat terlepas dan jatuh pada tempat yang sesuai yang akan tumbuh menjadi koloni likenes yang baru. Jalinan kecil hifa jamur-alga ini disebut dengan soredium.
Likenes sangat peka terhadap pencemaran oleh berbagai jenis zat berbahaya seperti logam berat, flourida, pestisida, radioaktif, karbon monooksida, dan zat lainnya sehingga likenes disebut sebagai tanaman indikator lingkungan. Apabila terdapat lingkungan yang tercemar oleh limbah maka likenes akan mati atau tidak tumbuh sama sekali.
Beberapa jenis likenes yang banyak dijumpai di atas bebatuan maupun pepohonan di hutan yaitu :
- Usnea dasypoga dan Usnea berbata, dugunakan sebagai bahan ramuan obat tradisional. Usnea mengahasilkan asam usnin yang berguna untuk melawan kuman penyakit.
- Cladonia rangiferina merupakan makanan utama rusa kutub.
- Roccelia tinctoria, sebagai bahan pembuat kertas lakmus
- Certraria islandica merupakan bahan ramuan obat – obatan
- Permelia acetabulum hidup pada pohon berupa lembaran – lembaran seperti kulit.
Hukum – Hukum Dasar Kimia
Hukum – Hukum Dasar Kimia
Hukum – Hukum Dasar Kimia
Hukum dasar kimia adalah hukum yang menjelaskan tentang dasar – dasar perhitungan kimia dalam aplikasi kimia, dikarenakan dalam setiap reaksi kimia yang kita buat dan tentukan berdasarkan atas hukum – hukum dasar kimia. Berikut ini akan saya jabarkan dan saya jelaskan mengenai hukum – hukum dasar kimia.
A. Hukum Kekekalan Massa ( Hukum Lavoiser)
Hukum kekelan massa ini pertama kali diamati dan dikemukakan oleh Antoine Laurent Lavoiser pada tahun 1785 menemukan fakta bahwasanya pada reaksi kimia tidak terjadi perubahan massa suatu zat, massa zat sebelum dan sesuadah reaksi adalah sama dan selalu tetap.
Perubahan materi yang kita amati umumnya berlangsung dalam wadah terbuka. Jika hasil reaksi ada yang berupa gas (seperti pembakaran kertas) maka zat yang tertinggal menjadi lebih kecil daripada massa semula dan begitu pula sebaliknya.
Untuk lebih jelasnya perhatikan table pengamatan dibawah ini reaksi antara besi dan sulfur yang menghasilkan besi (II) sulfide
|
Massa Zat yang bereaksi ( gr) |
Massa Zat hasil Reaksi Besi (II) Sulfida (gr) | |
|
Massa Besi |
Massa Sulfur | |
|
14 |
8 | 22 |
|
28 |
16 |
44 |
| 42 | 24 |
66 |
| 56 | 32 |
88 |
Dari percobaan diatas maka dapat disimpulkan bahwasanya massa zat sebelum dan sesudah reaksi adalah sama ini dinamakan dengan hukum kekelan massa (hukum lavoiser)
Cotoh Soal 1 :
Dalam wadah tertutup 4 gram logam Natrium dibakar denagn oksigen menghasilkan natrium oksida, jika massa natrium oksida yang dihasilkan adalah 5,6 gram, berapakah massa oksigen yang dibutuhkan ?
Solusi :
mNa = 4 gram
mNaO = 5,6 gram
berdasarkan hukum kekekalan massa maka
Massa sebelum reaksi = Massa sesudah reaksi
mNa +mO2 = mNaO
mO2 = mNaO – mNa
= (5,6 – 4) gram
= 1,6 gram
Contoh soal 2 :
Pada pembakaran 2,4 gram magnesium di udara dihasilkan 4 gram oksida magnesium, berapa gram oksigen yang terpakai dalam reaksi itu ?
Solusi:
mMg = 2,4 gram
mMgO = 4 gram
Massa sebelum reaksi = Massa sesudah reaksi
m Mg + m O2 = m MgO
m O2 = m MgO – m Mg
= (4 – 2,4) gram
= 1,6 gram
B. Hukum Proust ( Hukum Perbandingan Tetap )
Hukum proust pertama kali dikemukakan oleh Joseph Louis Proust pada tahun 1799 menyatakan bahwa perbandingan massa unsure – unsure dalam suatu senyawa adalah tertentu dan tetap.
Bagaimanakah dengan proses pembentukkan senyawa? Apakah perbandingan zat – zat yang beraksi juga tetap?perhatikan data pembentukkan senyawa air dari gas hidrogen dan oksigen pada table berikut.
|
Massa unsur – unsur pembentuk (gram) |
Massa senyawa air (gram) | |
|
Massa Hidrogen |
Massa Oksigen | |
|
1,0 |
8,0 |
9 |
|
1,5 |
12 |
13,5 |
|
2,0 |
16 |
18,0 |
| 2,5 | 20 |
22,5 |
| 3,0 | 24 |
27,0 |
Dari data diatas di dapatkan rumus antara lain
Massa B dalam AxBy = y x Ar B x Masa AxBy
MrAxBy
% B dalam AxBy = y x Ar B x % AxBy
MrAxBy
% Zat dalam campuran = Banyaknya zat x 100 %
Banyaknya Campuran
Contoh soal 1 :
Pada reaksi antara logam magnesium sebanyak 10 gram dengan 6 gram oksigen sesuai persamaan reaksi :
2 Mg (s) + O2 (g) ——– > 2 MgO (s)
Ternyata dari percobaan dihasilkan 15 gram magnesium oksida dan sisa logam magnesium sebanyak 1 gram, berapakah massa oksigen dan massa Magnesium pada magnesium oksida ? ( Ar Mg = 24, Ar O = 16)
Solusi :
Dari persamaan reaksi diatas maka kita bisa tentukan menggunakan rumus hukum proust yaitu.
Massa O dalam MgO = = (Ar O)/(Mr MgO) x massa MgO
= 16/40 x 15 gram
= 6 gram
MassaMg dalam MgO = (Ar Mg) / (Mr MgO) x massa MgO
= 24/40 x 15 gram
= 9 gram
Jadi massa magnesium yang bereaksi adalah 9 gram (tersisa 1 gram) dan massa oksigen yang bereaksi adalah 6 gram
Contoh soal 2 :
Suatu senyawa oksida besi (FeO) memiliki perbandingan massa besi dan oksigen sebesar 7 : 2. Tentukan persen massa dari besi dan oksigen dalam senyawa tersebut.
Solusi :
Total perbandingan 7 + 2 = 9
Persen massa besi = (perbandingan Besi)/(total perbandingan)x 100 %
= 7/9 x 100 %
= 77,8 %
Persen massa oksigen = (perbandingan oksigen) ∕ (total perbandingan) x 100 %
= 2/9 x 100 %
= 22,2 %
Contoh Soal 3 :
Perbandingan massa carbon terhadap oksigen dalam karbon dioksida adalah 3 : 8. Berapa gram karbon dioksida dapat dihasilkan apabila 6 gram karbon dengan 16 gram oksigen ?
Solusi :
Reaksi yang terjadi adalah C + 2 O ——– > CO2
Maka massa zat sebelum dan sesudah reaksi adalah sama
C : 2 O = 6 : 16 sehingga C : O = 6 : 8
Oksigen berlebih sehingga karbon habis bereaksi
Massa karbon yang bereaksi ( C ) = 6 gram
Massa oksigen yang bereaksi ( O ) = 8/3 x 6 gram
= 16 gram
Maka karbon dioksida yang dapat dihasilkan adalah 6 gram C + 16 gram O2 = 22 gram
C. Hukum Dalton (Hukum Perbandingan Berganda )
Hukum dalton berbunyi jika dua unsure membentuk dua macam senyawa atau lebih, untuk massa salah satu unsure yang sama banyaknya, maka massa unsure ke dua dalam senyawa – senyawa itu akan berbanding sebagai bilangan bulat sederhana.
Menurut teori atom Dalton senyawa terbentuk dari gabungan atom – atom dalam perbandingan sederhana. Misalkan unsure X dan Y membentuk dua jenis senyawa XY dan X2Y3. Jika massa unsure X dibuat sama ( berarti jumlah atomnya sama) maka rumus senyawa XY dapat ditulis sebagai X2Y2.
XY ——- > X2Y2
X2Y2 tetap sebagai X2Y3
Berarti perbandingan unsure Y dalam senyawa I dan II adalah 2 : 3
Untuk lebih jelas bisa perhatikan contoh soal dibawah ini.
Contoh 1 :
Karbon dapat bergabung denganhidrogen dengan perbandingan 3 : 1 membentuk gas metana berapa massa hidrogen yang diperlukan untuk bereaksi dengan 900 gram C pada metana ?
Solusi :
C : H = 3 : 1
Maka massa H = 1/3 x 900 gram
= 300 gram.
Contoh 2 :
Unsur A dan unsure B membentuk 2 senyawa yaitu X dan Y. Massa unsure A dalam senyawa X dan Y berturut – turut adalah 46,7 % dan 30,4 %. Tunjukkanlah bahwa hukum Dalton berlaku pada kedua senyawa tersebut ?
Solusi :
|
Senyawa |
% A | % B = 100 – % A |
|
X |
46,7 % |
100 – 46,7 % = 53,3 % |
| Y | 30,4 % |
100 – 30,4 % = 69,6 % |
Agar persentase A sama maka senyawa X dikalikan factor 2,14 dan senyawa Y dikalikan factor 3,28 sehingga diperoleh perbandingan massa X dan Y sebagai berikut :
|
Senyawa |
Massa X (gr) | Massa Y (gr) |
|
X |
46,7 x 2,14 = 100 |
53,3 x 2,14 = 114,06 |
| Y | 30,4 x 3,28 = 100 |
69,6 x 3,28 = 228,28 |
Jadi dapat diketahui perbandingannya X : Y = 114,06 : 228,28 = 1 : 2
Berdasarkan tiga hukum diatas yaitu hukum kekelan massa, hukum perbandingan tetap, hukum kelipatan perbandingan maka pada tahun 1803 Jhon Dalton mengemukakan suatu teori yang kita kenal dengan teori atom Dalton. Antara lain postulatnya sebagai berikut :
- Materi terdiri dari partikel yang sudah tidak terbagi, yaitu atom
- Atom – atom dari unsure yang sama adalah identik tetapi berbeda dengan atom unsure lain.
- Reaksi kimia adalah penggabungan, pemisahan atau penataan ulang dari atom – atom dalam jumlah sederhana.
D. Hukum Gay – Lussac ( Hukum Perbandingan Volume )
Hukum ini menjadi dasar bagi stoikiometri raeksi – reaksi gas. Yaitu yang berbunyi Volume gas – gas yang bereaksi dan volume gas hasil reaksi , jika diukur dalam tekanan dan suhu yang sama maka akan berbanding lurus sebagai bilangan – bilangan bulat sederhana.
Perbandingan volume gas sesuai dengan perbandingan koefisien reaksinya.
Maka akan di dapatkan rumus seperti berikut ini.
Volume gas yg dicari = (koefisien yang dicari)/(koefisien yang diketahui) X volume yang diketahui
Untuk lebih jelasnya perhatikan contoh soal dibawah ini.
Contoh 1 :
Sebanyak 8 L C3H8 dibakar habis dengan oksigen sesuai dengan persamaan reaksi
C3H8 + 5O2 ———- > 3CO2 + 4 H2O pada suhu dan tekanan yang sama volume gas CO2 yang dihasilkan adalah ?
Solusi :
Volume CO2 = (koefisien CO2)/(koefisien C3H8) X volume C3H8
= 3/1 X 8 L
= 24 L
Contoh 2 :
Jika 50 mL gas CxHy dibakar dengan 250 mL oksigen, dihasilkan 150 mL karbon dioksida dan sejumlah uap air. Semua gas diukur pada suhu dan tekanan yang sama. Tentukan rumus CxHy.
Solusi :
Perbandingan volume gas sesuai dengan perbandingan koefisiennya.Perbandingan volume yang ada disederhanakan, kemudian dijadikan sebagai koefisien. Perhatikan reaksi berikut ini.
CxHy + O2 ———– > CO2 + H2O
50 mL 250 mL 150 mL
1 2 3
Karena koefisien H2O belum diketahui , dimisalkan koefisien H2O adalah z maka didapatkan persamaan reaksi
CxHy + 5 O2 ———- > 3 CO2 + z H2O
∑ atom ruas kiri = ∑ atom ruas kanan
Berdasarakan jumlah atom O, 10 = 6 + z
z = 10 – 6 = 4
Sehingga persamaan reaksinya menjadi :
CxHy + 5 O2 ———- > 3 CO2 + 4 H2O
Untuk menentukan x dan y dilakukan penyetaraan jumlah atom C dan H
∑ atom ruas kiri = ∑ atom ruas kanan
Jumlah atom C = x =3
Jumlah atom H = y = 8
Jadi didapati rumus CxHy adalah C3H8
Contoh 3 :
Suatu campuran yang terdiri dari metana (CH4) dan etena (C2H4) dibakar sempurna menghasilkan karbon dioksida dan air. Pada suatu percobaan pembakaran 10 mL (T,P) campuran menghasilkan 16 mL (T,P) karbon dioksida. Tentukanlah susunan campuran tersebut.
Solusi :
Dari soal diatas pertama kita buat persaman reaksinya terlebih dahulu
CH4 + O2 —————– > CO2 + 2 H2O
C2H4 + 3 O2 —————– > 2 CO2 + 2 H2O
Lalu kita misalkan :
V C2H4 = x mL
V CH4 = ( 10 – x ) mL
Maka x mL C2H4 akan menghasilkan gas CO2 sebanyak = 2/1 . x mL = 2x mL
Sedangkan (10 – x ) mL CH4 akan menghasilkan gas CO2 sebanyak (10 – x)mL, dikarenakan hasil pembakaran kedua jenis gas adalah 16 mL maka akan didapatkan persamaan sebagai berikut :
2x mL – (10 – x) mL = 16 mL
2x mL – x mL = 16 – 10
X = 6 mL
Jadi campuran tadi akan menghasilkan gas antara lain 6 mL C2H4 dan 4 mL CH4 ( didapatkan dengan memasukkan harga x kedalam persamaan tiap gas yang telah dibuat di awal ).
E. Hukum Avogadro ( Hipotesis Avogadro )
Pada tahun 1811 seorang ilmuan dari Italia Amedeo Avogadro mengemukakan bahwasanya partikel unsur tidak harus berupa atom yang berdiri senidri akan tetapi dapat juga berupa gabungan dari beberapa atom yang disebut dengan molekul unsure.
Avogadro mengemukakan suatu hipotesis sebagai berikut “ Pada suhu dan tekanan yang sama, semua gas bervolume sama mengandung jumlah molekul yang sama pula.”
Sebagai contoh saya asumsikan sebagai berikut apabila saya mempunyai 2 buah tempe dan satu buah minyak goreng maka yang terbentuk adalah dua buah tempe goreng. Hipotesis ini menyerupai seperti yang dilakukan oleh Avogadro
Berdasarakan analogi diatas maka Avogadro mengemukakan rumusan tentang hukum Avogadro seperti berikut ini.
(Jumlah molekul x) / (Jumlah molekul y) = (Volume gas x ) / (volume gas y)
Pada suhu dan tekanan yang sama, perbandingan volume gas sesuai dengan perbandingan jumlah molekul dan sesuai dengan perbandingan koefisien reaksinya.
Dari pernyataan diatas maka didapatkan rumus
Volume yang dicari = (koefisien yang dicari) / (koefisien yang diketahui) X volume yang diketahui
Jumlah molekul yg dicari = (koefisien yang dicari) / (koefisien yang diketahui) X Jumlah molekul yang diketahui
Agar lebih jelas perhatikan contoh soal berikut ini :
Contoh soal 1 :
Sebanyak 35 L gas karbon dioksida mengandung 4,5 x 1023 molekul pada suhu dan tekanan yang sama, tentukan :
- Jumlah molekul 7 L gas hidrogen
- Volume gas amoniak yang mengandung 9 x 1023 molekul
Solusi :
- Jumlah molekul H2 = (volume H2) / (Volume CO2) X jumlah molekul CO2
= (7 L) / (35 L) X 4,5 x 1023 molekul
= 0,9 x 1023 molekul
= 9 x 1022 molekul
Jadi 7 L hidrogen mengandung 9 x 1022 molekul
2. Volume NH3 = (jumlah molekul NH3)/(jumlah molekul CO2) X volume CO2
= 9 x 1023 molekul / 4,5 x 1023 molekul X 35 L
= 70 L
Jadi 9 x 10 23 molekul gas amoniak memiliki vlume sebesar 70 L
Sistem Hormonal Pada Manusia
Sistem Hormonal Pada Manusia
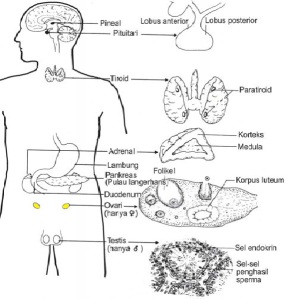
Hormon adalah suatu senyawa organic yang dihasilkan oleh kelenjar tertentu dan berfungsi untuk mengaktifkan suatu proses fisiologis dalam tubuh (metabolisme, pertumbuhan dan perkembangan, reproduksi dan reaksi terhadap stress serta tingkah laku). Kelenjar yang menghasilkan hormon dinamakan dengan kelenjar endokrin atau kelenjar buntu. Hormon merupakan senyawa steroid ataupun senyawa potein.
Hormon dapat digolongkan menjadi tiga kelompok yaitu :
- Hormon – hormon dari asam amino, misalnya tiroksin, triiodotironin, adrenalin, nonadrenalin.
- Hormon – hormon peptide dan protein, misalnya paratiroid, hormon pertumbuhan, insulin, glucagon.
- Hormon – hormon steroid, misalnya kortikosteroid dan hormon kelamin (androgen, estrogen, dan progesterone)
Berikut ini beberapa factor yang mempengaruhi pengatur sekresi hormon antara lain :
- Faktor Saraf
Bagian medulla kelenjar suprarenal mendapat pelayanan dari saraf ototnom. Oleh karena itu sekresinya diatur oleh saraf otonom.
- Faktor Kimia
Susunan bahan kimia atau hormon lain atau hormon lain di dalam aliran darah mempengaruhi sekresi hormon tertentu.
Hormon dikeluarkan sebagai akibat dari rangsangan stimulasi saraf secara langsung kepada kelenjar yang cocok. Macam – macam kelenjar endokrin pada manusia antara lain hipofisis, tiroid, paratiroid, timus, pankreas, adrenal, dan ovum atau testis.
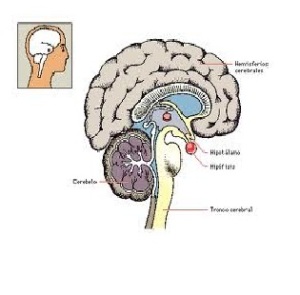
Hipotalamus
Hipotalamus memegang peranan yang sangat penting dalam pengaturan system endokrin dan system saraf. Hipotalamus menerima informasi dari system saraf melalui tubuh dan bagian otak, kemudian mengatur system endokrin untuk menanggapi kondisi lingkungan. Hormon yang dikeluarkan oleh hipotalamus merupakan sekresi dari sel – sel neurosekretori.
Kelenjar Hipofisis (Pituitari)
Kelenjar hipofisis dinamakan juga dengan master of gland dikarenakan hormon yang dihasilkan oleh hipofisis mempengaruhi pengeluaran hormon yang lain, hormon ini terbagi atas 3 macam bagian antara lain bagian anterior, bagian intermediet dan bagian posterior. Berikut saya jabarkan bagian dan fungsi dari hipofisis
|
No |
Kelenjar |
Letak |
Hormon |
Fungsi / Peran |
| 1 | Hipofisis / Pituitari | Sella tursica | metabolisme, pertumbuhan dan perkembangan, reproduksi dan reaksi terhadap stress serta tingkah laku | |
|
Pada lekukan tulang selatursika | GH / STH (Hormon somatotrof) | Pertumbuhan sel tubuh dan menstimulasikan pertumbuhan tulang | |
| TSH (hormone tiroid) | Mengontrol sekresi hormon oleh kelenjar tiroid | |||
| ACTH (hormone adrenokortil kotropik ) | Merangsang produksi glukokortikoid | |||
| FSH (Folikel stimulating Hormon) |
|
|||
| LH (Luteinizing hormone) |
|
|||
| Prolaktin | Membantu proses persalinan dan menstimulasi sekresi air susu. | |||
|
Pada lekukan tulang selatursika | MSH (Melanocyte Stimulating Hormone) | Mengatur pigmentasi dan mempengaruhi warna kulit. | |
|
Pada lekukan tulang selatursika | Oksitosin | Menstimulasikan kontraksi sel otot polos pada rahim wanita hamil selama melahirkan dan merangsang kontraksi sel – sel kontraktil dari kelenjar susu agar mengeluarkan air susu. | |
| ADH (Anti Deuretic Hormon) | Mencegah pembentukkan urin dalam jumlah banyak dan meningkatkan tekanan darah dengan menyempitkan pembuluh darah. |
Kelenjar Tiroid / gondok
Kelenjar tiroid adalah kelenjar yang terdapat di leher bagian depan dibawah jakun dan terdiri atas dua buah lobus berfungsi sebagai pengatur metabolisme sel tubuh dan pengaturan suhu tubuh, terdiri dari asam amino yang mengandung yodium. Berikut akan saya jabarkan fungsi dan bagiannya dalam table.
|
Hormon |
Fungsi / Peran |
| Tiroksin | Mengatur proses metabolisme, pertumbuhan fisik, perkembangan mental, kematangan seks, dan mengubah glikogen menjadi gula dalam hati serta pendistribusian air dan garam mineral. |
| Triodotironin | Mengatur metabolisme, dan kegiatan system saraf. |
| Kalsitonin | Menjaga kesetimbangan kalsium didalam darah dengan mempercepat penyerapan kalsium oleh tulang. |
Kelenjar Paratiroid / Anak Gondok
Kelenjar paratiroid terletak dibagian belakang kelenjar tiroid, kelenjar ini berjumlah empat buah kelenjar ini menghasilkan Hormon PTH ( Parathyroid Hormone) yang berfungsi meningkatkan serta mengendalikan kadar kalsium dalam darah dan fosfat (PO43+) dalam darah.
Kelenjar Timus / Kacangan
Kelenjar ini hanya dijumpai pada anak – anak usia di bawah 18 tahun. Kelenjar ini terletak didekat tulang dada dan berwarna kemerah – merahan, kelenjar ini terdiri atas 2 lobus. Kelenjar ini menghasilkan Hormon Thymosin yang berfungsi sebagai perangsang perkembangan dari limfosit T untuk menghasilkan kekebalan (imunitas) tubuh.
Kelenjar Adrenal / Anak ginjal
Kelenjar Adrenal berjumlah dua buah dan terdapat pada bagian atas ginjal kelenjar ini terbagi menjadi dua bagian yaitu korteks dan medula suprinalis, berikut akan saya jelaskan dalam table peran dan fungsinya.
|
Bagian |
Hormon |
Fungsi dan |
| Korteks | Glukokortikoid | Meningkatkan kadar glukosa dalam darah melalui perubahan glikogen dalam hati menjadi glukosa dalam darah. |
| Androgen | Bekerja sama dengan hormon yang dihasilkan gonad untuk menentukan sifat dan karakter kelamin sekunder. | |
| Mineralkortikoid | Mengatur volume darah, tekanan darah, serta kadar natrium (Na+) dan kalium (K+) dalam darah. | |
| Medula Suprenalis | Adrenalin (epineferin) | Membantu metabolisme dengan mengubah glikogen dalam otot menjadi glukosa dalam darah. |
| Nonadrenalin (norepineferin) | Menaikan tekanan darah dengan jalan merangsang serabut otot di dalam dinding pembuluh darah untuk berkontraksi. |
Kelenjar Pinealis ( Epifise )
Klenjar pinealis terletak di dekat otak, tepatnya diatas otak kecil ( cerebellum ). Kelenjar ini sangat kecil sebesar biji kacang ercis. Kelenjar ini menghasilkan Hormon Melatonin yang berfungsi dalam pengaturan hubungan suhu tubuh dengan tidur.
Kelenjar Pankreas / Langerhans
Kelenjar ini terdapat di dekat usus 12 jari dan hati. Didalam pankreas terdapat pulau – pulau langerhans, pulau langerhans ini mengandung sel – sel endokrin yaitu sel alfa yang menghasilkan hormon glukagon dan sel beta yang menghasilkan hormon insulin, berikut akan saya jabarkan di dalam table fungsi dan bagiannya
|
Bagian Sel |
Hormon |
Fungsi dan Peranan |
| Sel alfa | Glukagon | Mengubah glikogen menjadi glukosa |
| Sel beta | Insulin | Mengubah gula darah ( glukosa ) menjadi gula otot ( glikogen ) di hati sehingga mengurangi kadar gula dalam darah. |
Kelenjar Kelamin / Gonad
Kelenjar kelamin terbagi atas dua yaitu kelenjar kelamin pada wanita dan pada pria berikut akan saya jelaskan dalam table bagian dan fungsinya.
|
Kelamin |
Hormon |
Fungsi dan Peranan |
| Pria | Testosterone | Menentukan ciri pertumbuhan kelamin sekunder pada pria. |
| Wanita | Progesterone | Penebalan dinding rahim (endometrium) agar siap menerima sel telur yang sudah mengalami pembuahan. |
| Estrogen | Proses pembentukan dan pematangan sel ovum (sel telur) serta pengatur cirri kelamin sekunder pada wanita. |
Sistem Koordinasi Pada Manusia
Sistem Saraf
Sistem saraf adalah suatu bentuk system dalam organ manusia yang menghimpunan rangsangan dari luar lingkungan, mengubah rangsangan menjadi impuls saraf dan meneruskan impuls ini ke suatu daerah penerimaan dan korelasi yang terorganisasi dengan baik.
Impuls – impuls ini ditelah/diartikan dan selanjutnya dikirim ke organ – organ efektor untuk memberikan jawaban yang tepat. Fungsi ini dilaksanakan oleh sel yang sangat terspesialisasi yang benama neuron.
Sistem saraf berfungsi menerima, menghantarkan dan menanggapi rangsang. Sistem saraf tersusun dari sel – sel saraf neuron. Sel – sel ini terbagi atas menjadi beberapa macam antara lain bisa dilihat dari table yang saya buat :
|
Sel Saraf |
Bagian – Bagian Sel |
Fungsi |
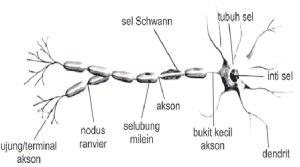
| Badan Sel | Membran Sel | Menerima implus dari dendrite untuk meneruskan rangsangan ke kelenjar otot atau sel saraf lainnya.Bagian badan sel yang berhubung dengan akson berbentuk segitiga yang bernama Akson Hillock |
| Sitoplasma | ||
| Nukleus | ||
| Nukleolus | ||
| Retikulum Endoplasma | ||
| Dendrit | Tonjolan Sitoplasma | Merupakan serat – serat yang melekat pada sel yang berfungsi sebagai penerima rangsang yang selanjutnya rangsang tersebut diubah menjadi impuls |
| Akson (Neurit) | Telodendron | Bagian terminal akson yang merupakan percabangan dari badan sel yang berfungsi untuk meneruskan rangsangan ke kelenjar saraf atau sel saraf lainnya. |
| Neurilema | Merupakan selaput tipis terdiri atas lemak yang berfungsi melindungi neurit dan menyelubungi akson | |
| Sel Schwan | Sel ini membentuk mielin untuk menutupi bagian bagian akson / membungkus akson | |
| Nodus Ranvier | Yaitu bagian akson yang tidak tertutupi oleh mielin. | |
| Sinapsis | Suatu sel saraf yang behubungan dengan sel saraf lainnya melalui suatu sambungan. Dalam sinapsis akan dikeluarkan senyawa kimia ( neuro – transmitter ) yang berfungsi menghantarkan impuls rangsang. |
Berdasarkan atas fungsinya neuron dapat dikelompokkan menjadi tiga macam yakni neuron sensoris, neuron motorik, neuron intermediet/konektor. Berdasarkan atas bentuknya neuron terbagi atas 3 macam yaitu neuron unipolar, neuron bipolar dan neuron bipolar, berikut akan saya jelaskan dalam table.
Neuron berdasarkan fungsinya :
|
No |
Bagian Neuron |
Ciri – ciri dan Fungsinya |
| 1 | Neuron Sensorik | Badan selnya bergerombol membentuk ganglia, aksonnya pendek sedangkan dendritnya panjang. Sel Neuron Sensorik ini berfungsi sebagai pembawa rangsangan dari sel saraf yang menerima rangsang (reseptor) ke system saraf pusat. |
| 2 | Neuron Motorik | Neuron ini memeiliki dendrite pendek dan akson panjang. Neuron ini berfungsi membawa atau meneruskan rangsangan dari system saraf pusat ke efektor atau organ gerak (otot dan kelenjar) |
| 3 | Neuron Intermediet / Konektor | Neuron ini memiliki dendrite yang pendek , aksonnya ada yang panjang dan ada yang pendek. Berfungsi menghantarkan rangsang dari neuron sensorik ke neuron motorik. |
Berdasarkan atas bentuknya antara lain yaitu
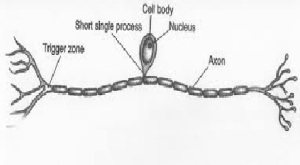
- Sel Saraf Unipolar
Yaitu sel saraf yang hanya mempunyai satu juluran badan sel yang bercabang menjadi akson dan dendrite. Perhatikan gambar dibawah ini.
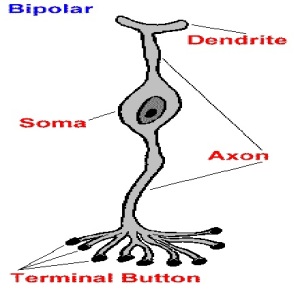
- Sel Saraf Bipolar
Yaitu sel saraf yang badan selnya memiliki dua juluran dendrite dan akson.
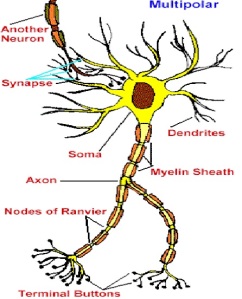
- Sel Saraf Multipolar
Yaitu sel saraf yang memiliki badan sel dengan banyak juluran dendrite dan satu juluran akson.
Penghantar Impuls
Impuls dalam suatu sel saraf berjalan dari dendrite, badan sel , dan sepanjang akson yang melalui selubung myelin, sel saraf yang satu dengan sel saraf lainnya mengadakan hubungan. Tempat hubungan tersebut dinamakan dengan sinapsis
Berikut ini akan saya jelaskan mekanisme kerja sinaps
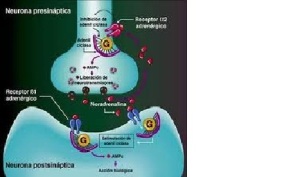
- Pada ujung akson (presinaps) terdapat membrane pemberi dan vesikula neurotransmitter dua bagian sel ini akan membentuk dan menghasilkan zat yang bernama zat neurotransmitter. Pada ujung dendrit (postsinaps)terdapat membrane penerima, diantara membrane pemberi dan membrane penerima terdapat celah sinapsn(synaptic cleft) yang berisi cairan asetilkolin.
- Apabila terdapat impuls masuk melalui bonggol sinaps gelembung – gelembung sinaps akan menghasilkan zat transmitter yang akan dilepaskan ke celah sinaps. Selanjutnya sampai ke sel saraf, apabila rangsang telah sampai ke presinaps maka presinaps akan menghasilkan enzim kolinase yang befungsi menghancurkan neurotransmitter pada celah sinaps.
Susunan System Saraf
Sistem saraf bekerja berdasarkan impuls elektrokimiawi. Sistem saraf berfungsi sebagai peninjau bagi tubuh dan pengumpul informasi tentang dunia luar maupun didalam tubuh. Selain itu berfungsi sebagai alat komunikasi umum, pusat pemetaan strategi, dan sebagai pembuat keputusan dalam segala sesuatu yang dilakukakn oleh tubuh. Pembagian system saraf pada manusia terbagi atas dua macam antara lain akan saya jabarkan satu persatu.
Saraf Pusat
Saraf pusat terdiri atas otak dan sumsum tulang belakang.Susunan system saraf pusat berfungsi sebagai penerima semua rangsang saraf dari luar tubuh (eksteroseptor) dan dari dalam tubuh (interoseptor), system saraf pusat juga bertindak sebagai pusat integrasi dan komunikasi.
Berikut akan saya jabarkan satu – satu mengenai saraf pusat
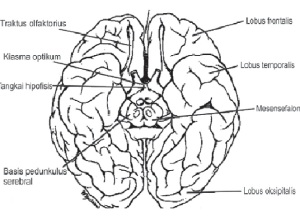
Otak
Otak merupakan pusat koordinasi dalam tubuh. Otak berada dalam rongga kepala yang dilindungi oleh pelapis otak yang disebut meninges. Pada meninges terdiri dari tiga macam lapisan yang urutan dari luar kedalamnya antara lain : Durameter (luar), Arachnoid (tengah), Piameter (dalam). Anatara piameter dan arachnoid atau durameter terdapat cairan limfe yang membesar yang berfungsi untuk memelihara sel- sel otak agar tetap basah, hal tersebut berkaitan dengan difusi oksigen dari pembuluh darah ke sel otak. Otak merupakan ujung anterior tabung neural yang membesar. Berikut akan saya jelaskan dalam bagan bagian – bagian dalam otak pada table berikut ini.
|
Lapisan |
Bagian |
Fungsi |
| Durameter (Lapisan Luar) | Selaput tulang Tengkorak | Selubung keras pembungkus otak yang berasal dari jaringan ikat tebal dan kuat. Yang mempunyai lapisan terpisah sebagai penghubung darah ke otak dan respon saraf. |
| Durameter propia | ||
| Kanal vertebralis | ||
| Longitudinal Superior | Mengalirkan darah dari vena ke otak | |
| Arachnoid (lapisan Tengah) | Selaput halus yang memisahkan durameter dan piameter,selaput membentuk sebuah kantong atau balon berisi cairan otak yang meliputi seluruh susunan saraf sentral. | |
| Saraf perifer | Mengambil cairan otak yang disebut fungsi lumbar | |
| Piameter (Lapisan Dalam) | Selaput tipis yang terdapat pada permukaan jaringan otak,berhubungan dengan arakhnoid melalui struktur – struktur jaringan ikat yang disebut dengan trabekel | |
| Kranium (rongga otak) | Bagian saraf sentral yang terletak di dalam rongga tengkorak | |
| Korteks ( kulit) | Memiliki banyak neuron terutama badan sel, dan dendrite | |
| Medulla (sumsum) | Banyak mengandung akson | |
| Ventrikel | Berisi cairan getah bening yang dinamakan serebrosipinal yang senantiasa membasahi otak` | |
| Korpus kalosum | Dinding yang melindungi otak dai goncangan |
Berikut akan saya jelakan dalam table bagian – bagian otak beserta fungsi – fungsinya
|
Posisi Otak |
Bagian Otak |
Fungsinya |
Penyakit yang terjadi |
| Otak depan |
|
||
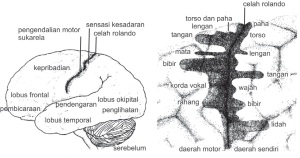
| Lobus Frontalis | Pengendali gerakan otot rangka dan tempat terjadinya intelektualitas.(fungsi motoris) | Epilepsi, Alzeihmer, Amnesia, Delesi Kepribadian. | |
| Lobus Oksipitalis | Pusat penglihatan | Kebutaan warna,geger otak, oksipitalis | |
| Lobus Temporalis | Sebagai pusat berbicara, penciuman, pengecap | Bisu dan tuli | |
| Lobus Parietalis | Perasa dingin, panas, sakit fisik dan pengatur perubahan kulit serta otot. | ||
|
Menerima rangsang serta serta melakukan persepsi rasa sakit dan menyenangkan | ||
|
Mengatur suhu tubuh, rasa lapar, emosi kadar air dalam tubuh, tekanan darah, rasa kantuk dan kadar gula dalam darah. | ||
|
Merupakan pangkal dari hipofisis yaitu hormon utama yang mengatur kegiatan dalam tubuh manusia. | ||
| Otak Tengah (mesensefalon | Korpus Kuadrageminus Superior | Mengatur mengangkat kelopak mata dan memutar bola tengah mata. | |
| Korpus Kuadrageminus inferior | Mengatur refleks mata dan kontraksi otot pergerakan mata. Dimana terdapat parietal corteks yang berfungsi sebagai perekam memori yang dilihat oleh mata. | ||
| Otak Belakang | Terdiri atas 3 macam bentuk : otak kecil, jembatan varol, sumsum lanjutan | ||
| Otak Kecil (serebrum) | Sebagai pusat keseimbangan, mengkordinasikan kerja otot, tonus otot, posisi tubuh, dan tulang, otak kecil menghubungkan jembatan varol dengan medulla oblongata melalui pedunkulus serebri inferior ( korpus retiformi) | ||
| Jembatan varol (pons Varolli) | Penghubung antara kedua bagian otak kecil ( vermis dan hemisfer), penghubung antara sumsum lanjutan dan serebrum / otak besar, pusat saraf nervus trigeminus. | ||
| Medula oblongata | Menghubungkan otak dengan sumsum tulang belakang sebagai pengatur denyut jantung, mengatur pelebaran dan penyempitan pembuluh darah, mengatur pernafasan,mengatur suhu tubuh,menelan,batuk, bersin, bersendawa, muntah serta merangsang otot – otot antar tulang rusuk dan diagfragma. | ||
| Sumsum Tulang belakang | Merupakan lanjutan dari sumsum lanjutan (medulla oblongata) yang berada dalam tulang belakang (canalis centralis vertebrta) | ||
| Sumsum tulang belakang (Canalis centralis vertebrata). | Berperan dalam gerak refleks serta menghubungkan saraf rangsang dari dan menuju otak. | ||
Sistem Saraf Tepi
System saraf tepi terbagi menjadi 12 pasang saraf otak dan 31 pasang saraf sumsum tulang belakang. Saraf tepi berfungsi sebagai penyampai informasi ke dan dari pusat pengatur.Berdasarkan impuls saraf yang dibawa saraf tepi dibedakan menjadi dua macam antara lain sebagai berikut :
- Sistem saraf aferen
Yaitu system yang berfungsi membawa impuls saraf dari reseptor ke susunan saraf pusat.
- System saraf eferen
Yaitu system yang berfungsi membawa impuls saraf dari saraf pusat ke efektor.
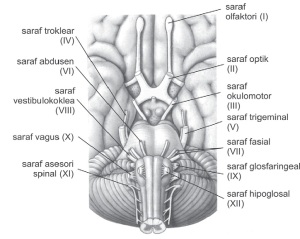
Untuk dapat memahaminya 12 macam pasang saraf akan saya buat di dalam tabel
|
No |
Nama Saraf |
Asal Saraf Sensori |
Asal Saraf Motorik |
|
1 |
Nervus Olfaktorius | Olifaktori otak menuju sel epitel Selaput lendir hidung sebagai indra pembau | Tidak ada |
|
2 |
Nervus Optikus | Optikus tengah yang menuju retina mata sebagai indra pelihat | Tidak ada |
|
3 |
Nervus Okulomotoris | Tidak ada | Otak tengah sebagai penggerak bola mata pengubah tebal lensa mata, penyempitan pupil dan sebagai penggerak mata ke kanan dan ke kiri. |
|
4 |
Nervus Trokhelearis | Tidak ada | Berasal dari otak tengah sebagai motoris menuju otot mata sebagai otot penggerak bola mata (obliks superior) |
|
5 |
Nervus Trigeminis | Dari tepi sumsum otak yang menuju lidah , gigi, kulit muka serta rahang sebagai indra pencium dan perasa serta penggerak lidah / pengunyah. | Tidak ada |
|
6 |
Nervus Faisalis | Berasal dari sumsum otak yang menuju muka sebagai indra perasa dan pengecap. Serta bibir pada muka. | Berasal dari sumsum otak yang menuju otot – otot muka sebagai pengatur mimik muka dan kelenjar ludah |
|
7 |
Nervus Abdusens | Berasal dari tepi sumsum otak yang menuju otot mata sebagai pemutar bola mata rektus eksternal. | Tidak ada |
|
8 |
Nervus Auditorius | Berasal dari tepi medulla otak yang menuju organ korti dalam koklea (rumah siput) dan saluran semisirkuler dalam alat keseimbangan | Tidak ada |
|
9 |
Nervus Vagus | Berasal dari tepi otak yang menuju faring,kantung suara, paru – paru, jantung, esophagus, usus halus dan lambung. | Menggerakan paru – paru, menggetarkan pita suara, kontraksi jantung, dan pengaruhi kinerja kerja gerak peristaltic. |
|
10 |
Nervus Glosofaringus | Berasal dari tepi medulla otak menuju lidah dan otot faring, berfungsi untuk mengecap rasa pada papilla lidah | Kelenjar parotis menuju otot penelan di dalam laring. |
|
11 |
Nervus Aksesorius | Tiak ada | Keluar dari otak yang menuju laring, pita suara, dan leher. Berfungsi sebagai penggerak otot faring, laring dan otot leher serta otot belikat. |
|
12 |
Nervus Hipoglosus | Tidak ada | Berasal dari dasar otak menuju otot lidah dan leher. Berfungsi sebagai penggerak otot lidah dan leher. |
Perhatikan Gambar dibawah ini
Berdasarkan atas kerjanya saraf tepi dibedakan menjadi dua macam yaitu saraf sadar (somatis) dan saraf tidak sadar (otonom), berikut ini akan saya jelaskan secara terperinci bagian – bagian pada saraf tersebut.
- Saraf Sadar (saraf somatis)
Saraf sadar adalah saraf yang rangsangannya disampaikan ke pusat reseptor yaitu ke pusat motoris pada serebrum.
- Saraf Tidak Sadar ( Otonom )
Yaitu saraf yang rangsangannya tidak disampaikan ke otak. Sistem saraf ini mengontrol organ – organ dalam tubuh dan otot polos pembuluh darah dimana otot polos pembuluh darah tersebut mengalami gerakan vasokontraksi dan vaso dilatasi (mengerut dan mengembang) saraf otonom bersifat motorik atau digolongkan kepada saraf aferen. Berdasarkan jenisnya dibedakan menjadi 2 macam yaitu :
Saraf Simpatik yang berfungsi mempercepat kerja organ – organ tubuh.
Saraf Parasimpatik yang berfungsi memperlambat kerja organ – organ tubuh.
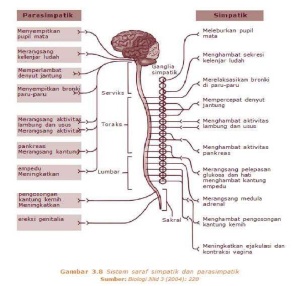
Efek yang berbeda ini disebabkan oleh neurotransmitter yang dihasilkan. Neurotransmitter saraf simpatik adalah noradrenalin, sedangkan neurotransmitter saraf parasimpatik adalah asetilkolin. Mengenai perbedaan saraf tersebut akan saya jabarkan pada table berikut ini.
|
Organ atau Jaringan |
Efek Stimulasi system saraf simpatik |
Efek stimulasi system saraf parasimpatik |
| Iris (pupil mata) | Melebarnya iris (pupil) | Menyempitkan iris (pupil) |
| Kelenjar air mata | Tidak ada | Menstimulasi keluarnya air mata |
| Kelenjar air liur | Menghambat sekresi air liur | Merangsang sekresi air liur |
| Otot antar tulang rusuk | Meningkatkan kecepatan bernafas | Mengurangi kecepatan bernafas |
| Bronkus dan Bronkeolus | Membesarkan bronkus dan bronkeolus | Mengecilkan bronkus dan bronkeolus |
| Jantung | Meningkatkan kecepatan denyut jantung | Menghambat kecepatan denyut jantung |
| Pembuluh darah | Meningkatkan tekanan darah | Menurunkan tekanan darah |
| System urin (kantung kemih) | Menurunkan pengeluaran urin | Meningkatkan pengeluaran urin |
| Usus | Menghambat gerak peristaltic, menghambat secresi getah lambung dan kontraksi sfingter dubur | Merangsang gerak peristaltic, merangsang getah lambung, merelaksaksi sfingter dubur. |
| Kulit | Kontraksi otot penegak rambut, merangsang produksi keringat, merangsng vasokontriksi yaitu mengecilnya diameter pembuluh darah biasanya pada arteriola | Merangsang vasodilatasi yaitu pembesaran diameter pembuluh darah biasanya terdapat pada arteriola |
Gerak Refleks
Gerak refleks adalah gerak spontan yang tidak melibatkan kerja otak, gerak ini dilakukan tanpa kesadaran dan gerak ini berguna untuk mengatasi kejadian yang tiba – tiba, gerak refleks juga dapat terjadi pada gerak yang rutin antara lain adalah gerak refles yang terjadi pada otot mata dan lutut.
Gerak refleks terbagi atas empat jenis,antara lain sebagai berikut :
- Refleks tunggal, yaitu terjadi apabila hanya memberikan sebuah respon
- Refleks ganda, yaitu terjadi apabila memberikan dua buah respon
- Refleks kompleks, yaitu jika respon yang diberikan lebih dari dua respon. Contohnya : seperti kaki terkena api maka akan segera ditarik, dipegang, menjerit.
- Refleks pelatihan (pelatihan yang diajari) yaitu suatu gerak refleks yang diajarkan secara terus menerus sehingga orang tersebut terlatih, Contoh : seorang atlit bela diri apabila dipukul maka dia dapat mengelakkan pukulan orang lain meskipun pukulan tersebut berasal dari belakang.
Sistem Pertahanan Tubuh
Sistem Pertahanan Tubuh
Sistem pertahanan tubuh berfungsi melindungi tubuh dari serangan benda asing atau bibit penyakit yang masuk ke dalam tubuh. Benda asing tersebut dapat berupa mikroorganisme penyebab penyakit ( pathogen) misal : virus, bakteri , jamur dan protozoa besel satu.
Sistem pertahanan tubuh terdiri atas 3 macam lapisan pertahanan antara lain dapat dilihat pada table beikut.
|
Pertahanan Tubuh Non Spesifik |
Pertahanan Tubuh Spesifik |
|
|
Lapisan Pertahanan Pertama |
Lapisan Pertahanan Ke Dua |
Lapisan Pertahanan Ke Tiga |
|
Kulit |
Sel Darah Putih Fagositik |
Limfosit |
|
Membran Mukosa |
Protein Anti Mikroba |
Antibodi |
|
Sekresi dari kulit dan Membran Mukosa |
Respon Peradangan |
|
Pada Lapisan pertama dikenal dengan sistem pertahanan tubuh nonspesifik eksternal dan pada lapisan pertahanan ke dua dikenal dengan sistem pertahanan tubuh nonspesifik internal untuk lebih dapat mengetahuinya bisa dilihat pada penjelasan dibawah ini.
Pertahanan Tubuh Non Spesifik Eksternal
Sistem pertahanan tubuh non spesifik merupakan pertahanan tubuh yang tidak membedakan mikroorganisme pathogen satu dengan yang lainnya.
1. Pertahanan yang terdapat di permukaan tubuh antara lain :
- Pertahanan fisik, dilakukan oleh kulit dan membran mukosa
- Pertahanan mekanis, dilakukan oleh rambut hidung dan silia
- Pertahanan kimiawi, dilakukan oleh sekret yang dihasilkan oleh rambut hidung dan silia.
- Petahanan biologis, dilakukan oleh populasi bakteri tidak berbahaya yang hidup di kulit dan membran mukosa.
Berikut ini saya jelaskan mengenai pertahanan tubuh nonspesifik eksternal.
Awal dari system pertahanan tubuh pada mahluk hidup adalah integumen atau penutup tubuh. Pada kulit mengeluarkan minyak dan keringat yang mengandung asam dan garam dengan pH berkisar antara 3 -5 kondisi ini dapat membunuh bakteri atau setidaknya mencegah banyaknya kolonisasi mikroorganisme di permukaan kulit.
Pada permukaan saluran pernafasan, usus, saluran pernafasan , system ekskresi, system reproduksi terdapat lapisan lendir (mucus).Membran mukosa juga mensekresikan mucus sehingga mampu membunuh mikrorganisme yang membahayakan tubuh. Pada mulut terdapat saliva (air liur) yang mengandung protein lisozim sebagai protein anti mikroba.Pada usus besar terdapat bakteri E. Coli yang menjadi pesing nutrisi bagi mikroorganisme pendatang baru.
Penelitian di jepang di bawah pimpinan Masatoshi Yamazaki menemukan adanya 14 jenis sayuran yang sering dikonsumsi masyarakat terdapat senyawa yang dapat menstimulasikan tubuh membentuk TNF (Tumor Necrosis Factor), yaitu senyawa yang aktif dalm meluruhkan sel tumor, selain itu senyawa yang terkandung dalam sayuran ini mampu menstimulasikan terbentuknya daya tahan tubuh yang disebut dengan Immunopotentiator. Hal ini juga didapatkan pada kopi senyawa kafein dengan ambang batas tertentu dapat membuat system imunal tubuh bekerja maksimal dengan bantuan co enzim pada substratnya.
Pertahanan Tubuh Nonspesifik Internal
2. Respon peradangan (inflamasi)
Inflamasi merupakan respon tubuh terhadap kerusakan jaringan, missal akibat tergores atau benturan keras. Pada proses ini dipengaruhi oleh Histamin dan Prostalgidin.
Histamin yang dihasilkan oleh sel tubuh berperan untuk meningkatkan konsentrasi otot dan permeabilitas dinding pembuluh darah kapiler di sekitar areal yang terinfeksi. Peningkatan aliran darah akan memudahkan perpindahan sel – sel fagosit dari darah ke dalam jaringan yang terluka Netrofil merupakan fagosit pertama yang menyelubungi luka selanjutnya monosit berperan dengan berkembang menjadi makrofag yang akan membersihkan sel – sel jaringan yang rusak.
3. Fagositosis
Fagositosis adalah suatu mekanisme pertahanan yang dilakukan oleh sel – sel fagosit dengan cara mencerna mikroorganisme / partikel asing yang masuk kedalam tubuh.
Fagiositosis dapat terjadi pada saat tubuh kita demam dikarenakan dalam sel darah putih melepaskan suatu senyawa yang disebut pirogen, pirogen akan meningkatkan suhu tubuh lebih tinggi karena proses respon sistemik yang dihasilkan oleh mikroorganisme pathogen.Proses tersebut membantu menghambat pertumbuhan mikroorganisme pathogen. Dengan kata lain demam dalam tingkat normal adalah proses imun tubuh dalam penghambat pertumbuhan mikroorganisme pathogen.
4. Protein anti mikroba
Jenis protein yang berperan dalam system pertahanan tubuh nonspesifik yaitu protein komplemen dan interferon, protein komplemen membunuh bakteri penginfeksi dengan cara membentuk lubang pada dinding sel dan membran plasma bakteri tersebut. Interferon akan membentuk zat yang mampu mencegah replikasi virus sehingga serangan virus dapat dicegah.
Pertahanan Tubuh Spesifik
Pada system pertahan tubuh ini bereaksi terhadap antigen dengan cara mengaktifasikan sel limfosit B yang akan mensekresikan protein khusus yang disebut antibody, setiap antigen memiliki susunan molekul khusus yang merangsang limfosit B tertentu untuk mensekresikan antibody yang berinteraksi secara spesifik dengan antigen tersebut.
Limfosit B dibentuk pada sumsum tulang kuning yang mengalami pembelahan atau diferensiasi menjadi sel plasma dan sel limfosit B ( didalam tubuh limfosit B jumlahnya mencapai 30% ). Sel plasma yang terbentuk bertugas menyekresikan antibody ke dalam cairan tubuh. Adapun limfosit B memori berfungsi menyimpan informasi antigen.
Limfosit T dibentuk dibentuk disumsum tulang akan tetapi pematangan llimfosit T terjadi di kelenjar timus, setelah mengalami pematangan limfosit T dan limfosit B akan masuk kedalam system peredaran limfatik, oleh karena itu sel – sel limfotik banyak ditemui pada peredaran darah limfatik,sumsum tulang, kelenjar timus, kelenjar limpa, amandel, darah dan system pencernaan.
Berikut akan saya jabarkan dalam table beberapa peranan dan fungsi limfosit .
|
Tipe Limfosit |
Jenis Limfosit |
Fungsi |
| Limfosit B ( sel B ) | Sel B plasma | Membentuk antibody. |
| Sel B pengingat | Mengingat antigen yang pernah masuk kedalam tubuh. | |
| Sel B pembelah | Membentuk sel B plasma dan sel B pengingat. | |
| Limfosit T ( sel T ) | Sel T pembunuh | Menyerang pathogen yang masuk kedalam tubuh, sel tubuh yang terinfeksi, serta sel kanker secara langsung. |
| Sel T pembantu | Menstimulasikan pembentukkan jenis sel T lainnya dan sel B plasma serta mengaktifasikan makrofag untuk melakukan fagositosis. | |
| Sel T Supresor | Menurunkan dan menghentikan respon imun dengan cara menurunkan produksi antibody dan mengurangi aktifitas sel T pembunuh. |
Antibody
Seperti yang telah dijelaskan sebelumnya bahwa limfosit B membentuk sel plasma yang akan mensekresikan antibody. Antibodi terdiri atas sekelompok protein serum globular yang disebut immunoglobulin. Protein ini merupakan protein khusus yang diimigrasikan atau dipindahkan ke bagian membrane sel, kemudian akan mengenali dan membunuh sel asing yang di temui.
Levine dan miller (1991 : 785) menjelaskan bahwa terdapat lima kelompok immunoglobulin yakni IgM, IgA, IgG, IgD dan IgE berikut akan saya jelaskan dalam table tipe – tipe antibody beserta karakteristiknya.
|
No |
Tipe Antibodi |
Karakteristik |
|
1 |
IgM |
Antibodi ini dilepaskan ke aliran darah pada saat terjadi infeksi yang pertama kali ( respon kekebalan primer ) |
|
2 |
IgG |
Antibodi ini banyak terdapat di dalam darah dan diproduksi saat terjadi infeksi kedua ( respon kekebalan sekunder ). IgG juga mengalir melalui plasenta dan memberi kekebalan pasif dari ibu dan janin. |
|
3 |
IgA |
Antibody IgA dapat ditemukan didalam air mata, air ludah, keringat dan membran mukosa. IgA berfungsi untuk mencegah infeksi pada permukaan epithelium. IgA juga terdapat dalam kolestrum yang berfungsi untuk mencegah kematian bayi akibat infeksi saluran pencernaan. |
|
4 |
IgD |
Antibodi ini ditemukan pada permukaan limfosit B sebagai reseptor dan berfungsi merangsang pembentukkan antibody oleh sel B plasma. |
|
5 |
IgE |
Antibodi ini ditemukan terikat pada basofil didalam sirkulasi darah dan mastosit di dalam jaringan yang berfungsi mempengaruhi sel untuk melepaskan histamin yang terlibat dalam reaksi alergi. |
Respon kekebalan tubuh terhadap antigen
Respon kekebalan tubuh terhadap antigen dapat dikelompkan menjadi dua macam yaitu kekebalan humoral ( antibody – mediated immunity ) dan kekebalan seluler ( cell – mediated immunity). Berikut akan saya jelaskan satu persatu respon kekebalan tubuh.
1) Kekebalan Humoral
Kekebalan humoral melibatkan aktivitas sel B dan antibody yang beredar dalam cairan darah dan limfe. Antibody yang beredar sebagai respon humoral bekerja melawan bakteri bebas, racun, virus dan mikroorganisme lainnya yang berada dalam cairan tubuh. Serangkaian respon terhadap pathogen ini disebut dengan respon kekebalan primer antara lain :
Netralisasi yaitu antibody akan menetralkan suatu virus dengan cara melekat pada molekul yang harus digunakan oleh virus untuk menginfeksi sel inang.mekanisme ini akan menetralkan racun dari mikroorganisme sehingga akan mudah difagositosis oleh makrofag.
Aglutinasi (penggumpalan) yaitu proses penggumpalan bakteri atau virus yang diperantarai oleh antibody yang akan bekerja menetralkan mikrorganisme tersebut. Terjadi karena setiap molekul antibody memiliki paling tidak dua tempat pengikatan antigen. Kompleks besar yang terbentuk melalui proses aglutinasi yang akan memudahkan fagositosis makrofag.
Presipitasi (pengendapan) yaitu proses dimana molekul – molekul antigen yang terlarut dalam cairan tubuh akan diendapkan oleh antibody. Proses ini akan memudahkan proses pengeluaran dan pembuangan antigen oleh fagositosis.
Fiksasi komplemen (aktivasi) yaitu mengaktivasikan komplemen dengan adanya kompleks antigen – antibody. Apabila ada infeksi maka protein yang pertama dalam rangkaian protein komplemen akan diaktifkan, reaksi komplemen ini akan mengakibatkan lisisnya banyak jenis virus dan sel – sel pathogen.
2) Kekebalan Seluler
Kekebalan seluler melibatkan sel T Yang bertugas menyerang sel – sel asing atau jaringan tubuh yang terinfeksi secara langsung seperti yang telah saya jelaskan sebelumnya diatas.
Berdasarkan cara memperolehnya kekebalan tubuh digolongkan menjadi dua kelompok yaitu kekebalan aktif dan kekebalan pasif.
1. Kekebalan Aktif
Kekebalan aktif merupakan kekebalan yang dihasilkan oleh tubuh itu sendiri, Tubuh membentuk antibody sendiri karena infeksi antigen. Kekebalan ini dapat diperoleh secara alami dan buatan sebagai contoh secara alami melalui penyakit seperti halnya penyakit cacar dan secara langsung tubuh membentuk vaksinasi virus cacar dengan cara didalam tubuh penderita dikembangkan kekebalan humoral dan kekebalan seluler, setelah mengidap penyakit cacar penderita tidak akan terkena dua kali penyakit cacar. Sedangkan cara buatan dengan adanya vaksinasi (imunisasi) terhadap mikroorganisme tertentu dengan cara dimasukkan antigen yang telah dilemahkan atau telah mati kedalam tubuh.
2. Kekebalan Pasif
Kekebalan pasif merupakan kekebalan yang diperoleh setelah menerima antibody dari luar. Kekebalan ini dapat diperoleh dengan cara alami yaitu dengan cara pemberian ASI ( Air Susu Ibu ) dan secara buatan melalui penyuntikkan antiserum yang mengandung antibody IgG atau immunoglobulin lainnya. Kekebalan pasif buatan ini hanya bertahan beberapa minggu saja karena immunoglobulin yang berasal dari tubuh akan diuraikan oleh tubuh orang tersebut.
Detik – Detik wafatnya rasulullah SAW
Detik-detik Menjelang Kematian Rasulullah
Pagi itu, Rasulullah dengan suara terbata-bata memberikan petuah: “Wahai umatku, kita semua ada dalam kekuasaan Allah dan Cinta Kasih-Nya.
Maka taati dan bertakwalah hanya kepada-Nya. Kuwariskan dua hal pada kalian, Sunnah dan Al-Qur’an. Barang siapa yang mencintai Sunnahku berarti mencintai aku, dan kelak orang-orang yang mencintaiku, akan bersama-sama masuk surga bersama aku,“
Khutbah singkat itu diakhiri dengan pandangan mata Rasullah yang teduh menatap sahabatnya satu persatu. Abu Bakar menatap mata itu dengan berkaca-kaca. Umar dadanya naik turun menahan nafas dan tangisnya. Ustman menghela nafas panjang dan Ali menundukan kepalanya dalam-dalam. (sesuai dengan kepribadian para sahabat Abu Bakar yg lembut hatinya, Umar yg kuat dan pemberani, ustman yg tabah,Ali yg cerdas…)
Isyarat itu telah datang, saatnya sudah tiba “Rasulullah akan meninggalkan kita semua” desah hati semua sahabat kala itu. Manusia tercinta itu, hampir usai menunaikan tugasnya di dunia.
Tanda-tanda itu semakin kuat, tatkala Ali dan Fadhal dengan sigap menangkap Rasulullah yang limbung saat turun dari mimbar. Saat itu, seluruh sahabat yang hadir di sana pasti akan menahan detik-detik berlalu, kalau bisa.
Matahari kian tinggi, tapi pintu rumah Rasulullah masih tertutup. Sedang di dalamnya, Rasulullah sedang terbaring lemah dengan keningnya yang berkeringat dan membasahi pelepah kurma yang menjadi alas tidurnya. Tiba-tiba dari luar pintu terdengar seseorang yang berseru mengucapkan
salam.
“Assalaamu’alaikum… .Bolehkah saya masuk ?” tanyanya. Tapi Fatimah tidak mengijinkannya masuk, “Maafkanlah, ayahku sedang demam” kata Fatimah yang membalikkan badan dan menutup pintu. Kemudian ia kembali menemani ayahnya yang ternyata sudah membuka mata dan bertanya kepada Fatimah. “Siapakah itu wahai anakku?”
“Tak tahulah aku ayah, sepertinya baru sekali ini aku melihatnya” tutur Fatimah lembut. Lalu Rasulullah menatap putrinya itu dengan pandangan yang menggetarkan. Satu-satu bagian wajahnya seolah hendak dikenang.
“Ketahuilah, dialah yang menghapuskan kenikmatan sementara, dialah yang memisahkan pertemuan di dunia. dialah Malaikat Maut,” kata Rasulullah.
Fatimah pun menahan ledakan tangisnya. Malaikat Maut datang menghampiri, tapi Rasulullah menanyakan kenapa Jibril tak ikut menyertai. Kemudian dipanggillah Jibril yang sebelumnya sudah bersiap diatas langit untuk menyambut ruh kekasih Allah dan Penghulu dunia ini. (sepertinya Malaikat Jibril Tidak Sanggup melihat Rasulullah dicabut nyawanya)
“Jibril, jelaskan apa hakku nanti dihadapan Allah?” Tanya Rasulullah dengan suara yang amat lemah. “Pintu-pintu langit telah dibuka, para malaikat telah menanti Ruhmu, semua pintu Surga terbuka lebar menanti kedatanganmu” kata Jibril. Tapi itu semua ternyata tidak membuat Rasulullah lega, matanya masih penuh
kecemasan.
“Engkau tidak senang mendengar kabar ini, Ya Rasulullah?” tanya Jibril lagi. “Kabarkan kepadaku bagaimana nasib umatku kelak?”
“Jangan Khawatir, wahai Rasulullah, aku pernah mendengar Allah berfirman kepadaku: ‘Kuharamkan surga bagi siapa saja, kecuali umat Muhammad telah berada didalamnya’” kata Jibril.
(subhanallah Beliau mencemaskan kita semua..amien) Detik-detik semakin dekat, saatnya Izrail melakukan tugas. Perlahan Ruh Rasulullah ditarik. Tampak seluruh tubuh Rasulullah bersimbah peluh, urat-urat lehernya menegang.
“Jibril, betapa sakit Sakaratul Maut ini.” Lirih Rasulullah mengaduh. Fatimah terpejam, Ali yang disampingnya menunduk semakin dalam dan Jibril memalingkan muka. “Jijikkah engkau melihatku, hingga kau palingkan wajahmu wahai Jibril?”
Tanya Rasulullah pada malaikat pengantar wahyu itu. “Siapakah yang tega, melihat kekasih Allah direngut ajal,” kata Jibril. Sebentar kemudian terdengar Rasulullah memekik karena sakit yang tak tertahankan lagi.
“Ya Allah, dahsyat nian maut ini, timpakan saja semua siksa maut ini kepadaku, jangan kepada umatku”. (Beliau Begitu Memikirkan
umatnya, Seharusnya bisa Saja Rasulullah Meminta untuk dihilangkan rasa sakitnya karena doa Beliau sungguh didengarkan oleh-Nya. Tetapi Beliau lebih Mengkhawatirkan Umatnya)
Badan Rasulullah mulai dingin, kaki dan dadanya sudah tak bergerak lagi. Bibirnya bergetar seakan hendak membisikan sesuatu, Ali segera mendekatkan telinganya. “Peliharalah shalat dan santuni orang-orang lemah diantaramu”
Di luar pintu, tangis mulai terdengar bersahutan, sahabat saling
berpelukan. Fatimah menutupkan tangan diwajahnya, dan Ali kembali mendekatkan telinganya ke bibir Rasulullah yang mulai kebiruan. “umatku, umatku, umatku”
dan……..
PUPUSLAH KEMBANG HIDUP MANUSIA MULIA ITU………
“Wahai Jiwa Yang Tenang
Kembalilah Kepada Tuhanmu
Dengan Hati Yang Puas Lagi Diridhai-Nya
Maka Masuklah Ke Dalam Jamaah Hamba-Hamba- Ku
Dan Masuklah Ke Dalam Jannah-Ku”
Sejarah Berdirinya Bimbel Az – Zahra
Sejarah Bimbel Az – Zahra
Dewasa ini perkembangan ilmu pengetahuan dalam era globalisasi menuntut kita untuk selangkah lebih maju dan memahami ilmu pengetahuan secara jelas, agar integritas sebuah bangsa dapat terwujud sehingga tercapainya bangsa yang maju. Oleh karena itu dibutuhkanlah sebuah lembaga yang mewadahi ilmu pengetahuan selain pendidikan formal baik sekolah maupun universitas. Karena dengan adanya ilmu pengetahuan kita dapat melihat secara jelas batasan – batasan antara logika dan kenyataan yang harus dihadapi oleh semua orang.
Fase manusia menjadi pribadi yang berhasil dalam setiap permasalahan didukung oleh ilmu pengetahuan yang ada dalam diri manusia tersebut. Yang merupakan kerangka dalam pembentukan pribadi yang maju. Seseorang yang memiliki dan menguasai ilmu pengetahuan akan selalu memiliki hidup yang penuh arti dan selalu siap menghadapi perkembangan zaman. Banyak orang yang tidak bisa menikmati pendidikan secara layak dan tidak bisa menghadapi kenyataan hidup karena minimnya pendidikan yang didapatinya sehingga manusia cenderung lebih pasrah dalam menghadapi keadaannya. Karena kenyatan – kenyataan itulah kami memberikan aspek dan sudut pandang yang transparan demi kebangkitan ilmu pengetahuan untuk setiap golongan masyarakat, sehingga terciptanya stabilitas tatanan manusia yang berfikir maju.
Atas dasar hal tersebut kami mendirikan bimbingan belajar untuk tiap lapisan masyarakat baik yang mampu ataupun yang tidak mampu, guna menumbuhkan rasa keingintahuan terhadap ilmu pengetahuan yang membawa mereka menjadi manusia yang maju dalam berfikir. Dan selaku pendidik ingin mambuntu adik – adik mewujudkan cita – citanya dengan membantu dalam proses belajar mengajar yaitu dengan cara mendirikan sebuah bimbel bernama Az – Zahra yang bertempat di Jln. H. Nasir Gg. Langgar Rt.009 / 005 N0. 27 Kel. Srengseng Kec. Kembangan Jakarta barat. Dibina dan diajarkan oleh guru – guru yang handal dibidangnya dan mempunyai system sarana diskusi, solusi soal sulit , proses pengerjaan PR / Tugas sekolah di luar jam bimbel dan pengajaran sesuai kurikulum serta penyampaian pelajaran yang membuat anak menjadi kritis.
Bimbel ini berdiri di tahun 2012 sampai sekarang ini sudah mempunyai 70 siswa dengan jenjang pendidikan yang berbeda – beda. Alhamdulillah di tahun ini kami sudah membantu siswa – siswa dalam menghadapi UN SD dan UN SMA. Saat ini kami sedang menjalani program persiapan SBMPTN ( Saringan Bersama Masuk Perguruan Tinggi Negeri ) dan persiapan SIMAK UI 2013.
Berikut ini adalah beberapa program yang kami selenggarakan:
- PAKET SIAP UAN ( SD, SMP, SMA )
- Bimbel ( SD, SMP, SMA )
- Persiapan SBNMPTN dan SIMAK UI
Jika berminat silahkan hubungi kontak person dibawah ini :
Alkaf Renaldy : 0812 – 9503 – 9816 Pin BB : 224CCD4D
Feby Triana : 0812 – 2442 – 2407 Pin BB : 33015B2A
Kelarutan dan hasil kali kelarutan (Ksp)
KELARUTAN DAN HASIL KALI KELARUTAN (Ksp)
Kelarutan ( solubility ) adalah suatu zat dalam suatu pelarut dimana menyatakan jumlah maksimum suatu zat yang dapat larut dalam suatu pelarut. Contoh bentuk kelarutan antara lain, apabila kalian ingin membuat teh manis pertama – tama kalian menuangkan gula kedalam gelas dan menuangkan air panas kedalam gelas yang telah berisi gula tersebut ketika kalian aduk sebelum mencelupkan teh celupnya maka kalian akan melihat adanya gula yang terlarut ( seperti adanya awan di dalam air ), apa yang akan terjadi apabila kalian menambahkan lagi gula kedalam air tersebut secara terus menerus apakah gula tersebut akan larut ? sebelum menjawab pertanyaan tadi mari kita pelajari kelarutan dibawah ini.
Besarnya kelarutan suatu zat dipengaruhi oleh beberapa faktor antara lain sebagai berikut :
1. Jenis Pelarut
Senyawa polar larut dalam pelarut yang polar dan begitu sebaliknya senyawa nonpolar akan larut dalam pelarut yang nonpolar.
2. Suhu
Kelarutan zat padat dalam air semakin tingi apabila suhunya dinaikkan.
Suatu kelarutan (khususnya untuk suatu zat yang sukar larut) dinyatakan dalam mol/L. Jadi kelarutan sama dengan kemolaran dari larutan jenuhnya.
Dalam hal ini terbagi atas 2 macam tipe larutan dalam suatu pelarut. Antara lain sebagai berikut:
A. Larutan Jenuh
Larutan jenuh adalah larutan yang telah mengandung zat terlarut dalam konsentrasi maksimum ( tidak dapat ditambah lagi )
Pada larutan jenuh akan terbentuk 2 hal antara lain
Konsentrasi maksimum zat terlarut = kelarutan (s)
Harga kesetimbangan = hasil kali kelarutan (Ksp)
Contoh : misalkan AgCl dilarutkan di dalam air akan terjadi reaksi ionisasi sebagai berikut
AgCl (s) <———— > Ag+(aq) + Cl–(aq)
Dari contoh tersebut maka akan didapatkan kesetimbangannya yaitu :
K = [Ag+] [Cl–] dimana pada larutan jenuh AgCl, konsentrasi ion Ag+ dan Cl– akan setara dengan harga kelarutan AgCl didalam air, sehingga harga K pada kesetimbangan kelarutan (garam atau basa yang sedikit larut) disebut hasil kali kelarutan dan dilambangkan dengan Ksp.
Pada elektrolit yang sukar larut di dalam air akan mengalami reaksi kesetimbangan
Contoh :
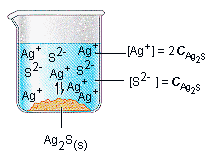
Ag2CO3 <———> 2 Ag+ (aq) + CO32- (aq)
Konsentrasi s ~ 2s ~ s
Ksp = [Ag+]2 [CO32-]
Ksp = [2s]2 [s]
Ksp = 4s3
Konsentrasi dalam larutan jenuh dinyatakan dalam symbol s
Contoh Soal :
1). Dalam 500 ml larutan dapat terlarut 0,65 gram Cu(IO3)2. Berapakah Ksp garam tersebut ? ( Ar O = 16 ; Cu = 63,5 ; I =127 )
2) Diketahui Ksp Ca(OH)2 = 5 X 10-6 tentukan pH larutan jenuh Ca(OH)2
Pengaruh ion senama / sejenis terhadap kelarutan
Sejauh ini kita telah membahas kelarutan elektrolit, akan tetapi seringkali terdapat sumber yang lain dari ion yang senama (sejenis) dalam larutan. Hal ini akan dibahas pengaruh ion sejenis.
Contoh : Jika AgCl dilarutkan dalam larutan NaCl atau larutan AgNO3 ternyata kelarutan AgCl dalam larutan tersebut lebih kecil jika dibandingkan dengan kelarutan AgCl di dalam air murni. Hal ini disebabkan karena pengaruh adanya ion senama (sejenis) yang ada didalam larutan tersebut. Ion Cl– dari NaCL atau ion Ag+ dari AgNO3 akan mempengaruhi laju kesetimbangan, sehingga kesetimbangan akan bergeser ke arah kiri.
Sesuai dengan asas Le Chatlier penambahan ion Ag+ atau Cl– akan menggeser kesetimbangan ke kiri sehingga AgCl yang larut semakin sedikit
AgCl(s) <————— > Ag+(aq) + Cl–(aq)
Jadi dengan adanya ion sejenis akan memperkecil kelarutan suatu elektrolit. Makin banyak ion sejenis yang ada dalam larutan maka akan semakin kecil kelarutan elektrolit tersebut.
Cara menghitung kelarutan elektrolit jika ada ion sejenis sebagai berikut :
- Melalui persamaan Ksp, hitunglah konsentrasi ion yang tidak memiliki ion sejenis
- Berdasarkan koefisien reaksi ionisasi, hitunglah kelarutan elektrolit
Berikut akan saya berikan table Ksp dari suatu larutan :
|
Larutan |
Kesetimbangan Larutan |
Ksp |
| Aluminium hidroksida | Al(OH) (s) < ———- > Al3+(aq) + 3OH–(aq) | 1,3 × 10–33 |
| Barium karbonat | BaCO3(s) < ———– > Ba2+(aq) + CO32–(aq) | 5,1 × 10–9 |
| Barium sulfat | BaSO4(s) < ———- > Ba2+(aq ) + SO42–(aq) | 1,1 × 10–10 |
| Kalsium karbonat | CaCO3(s) < ———– > Ca2+(aq) + CO32–(aq) | 2,8 × 10–9 |
| Kalsium flourid | CaF2(s) < ———— > Ca2+(aq) + 2F–(aq) | 5,3 × 10–9 |
| Kalsium sulfat | CaSO4(s) < ———– > Ca2+(aq) + SO42–(aq) | 9,1 × 10–6 |
| Kromium (III) hidroksida | Cr(OH)3(s) < ———- > Cr3+(aq) + 3OH–(aq) | 6,3 × 10–31 |
| Besi (III) hidroksida | Fe(OH)3(s) < ——— > Fe3+(aq) + 3OH–(aq) | 4 × 10–38 |
| Timbal (II) klorida | PbCl2(s) < ———– > Pb2+(aq) + 2Cl–(aq) | 1,6 × 10–5 |
| Magnesium karbonat | MgCO3(s) < ———- > Mg2+(aq) + CO3(aq) | 3,5 × 10–8 |
| Magnesium hidroksida | Mg(OH)2(s) < ——– > Mg2+(aq ) + 2 OH–(aq) | 1,8 × 10–11 |
Sumber: General Chemistry, Principles and Modern Application, Petrucci R. H, Harwood W. S, dan Herring G.F
Contoh soal 1 :
Diketahui harga Ksp AgCl sebesar 1,6 × 10–10. Tentukan kelarutan AgCl dalam larutan NaCl 0,04 M.
Solusi
Asumsikan bahwa NaCl terionisasi sempurna.
Ionisasi NaCl :
NaCl(aq) ————- > Na+(aq) + Cl–(aq)
0,04 M ~ 0,04 M ~ 0,04 M
Kesetimbangan AgCl :
AgCl(s) < —— > Ag+(aq) + Cl–(aq)
s ~ s ~ s
Dari reaksi di atas diperoleh [Ag+] = s
[Cl–] = (0,04 M + s), karena s << 0,04, maka [Cl–] = 0,04 M.
Kelarutan AgCl dalam NaCl 0,04 M dapat dihitung dengan cara berikut.
Ksp = [Ag+] [Cl–]
1,6 × 10–10 = (s) (0,04)
s = 4 × 10–11
Jadi, kelarutan AgCl dalam NaCl 0,04 M sebesar 4 × 10–11 M.
Contoh Soal 2:
Diketahui suatu larutan 100 ml CaF2 mempunyai Ksp 4 x 10-11 tentukan kelarutan CaF2 didalam larutan 0,01 M CaCl2 100 ml ?
Solusi
Dari sini kita bisa mengasumsikan bahwasanya terdapat ion senama sehingga CaCl2 terionisasi sempurna.
Ionisasi CaCl2 :
CaCl2 (aq) ———- >Ca2+ (aq) + 2 Cl– (aq)
0,01 M ~ 0,01 M ~ 0,02 M
Kesetimbangan CaF2 :
CaF2 (s) < ——- > Ca2+(aq) + 2 F– (aq)
s ~ s ~ 2s
Maka Berlaku :
[Ca2+] [ 2 Cl–] = Ksp CaCl2
[0,01] [2s]2 = 4 x 10-11
4s2 = 4 x 10-11 / 0,01
= 4 x 10-9
s2 = 10-9
s = √(10 x 10-9 )
s = 10-5
Jadi kelarutan CaF2 pada 0,01 M CaCl2 adalah 10-5 M
Defenisi Enzim
DEFENISI ENZIM & CARA KERJA ENZIM
A. Pengertian Enzim
- Enzim merupakan senyawa organik atau katalis protein yang dihasilkan oleh sel dan berperan sebagai katalisator yang dinamakan biokatalisator.
- enzim merupakan zat protein yang untuk sementara terikat satu atau lebih zat – zat yang bereaksi. Dengan demikian enzim menurunkan energy aktifasi pada sel atau organ dalam mahkluk hidup sehingga reaksi yang berlangsung cepat.
- Secara kimia enzim terdiri atas dua bagian (enzim lengkap/holoenzim), yaitu bagian protein (apoenzim) dan bagian bukan protein (gugus prostetik) yang dihasilkan dalam sel makhluk hidup.
B. Cara Kerja Enzim
Enzim bekerja mengkatalis reaksi dengan meningkatkan kecepatan reaksi. Meningkatkan kecepatan reaksi ini dilakukan dengan menurunkan energy aktifasi (energy yang dibutuhkan untuk reaksi).Penurunan energy aktifasi dilakukan dengan cara membentuk kompleks dan substrat.
Berikut merupakan cara kerja suatu enzim :
SUBSTRAT + ENZIM —–> (ENZIM + PRODUK) – SUBSTRAT
Setelah produk dihasilkan dari suatu reaksi enzim,enzim akan dilepaskan. Enzim bebas akan membentuk kompleks yang baru dengan substrat yang lain.
Agar dapat melakukan kerjanya suatu enzim tidak harus menyatu walaupun hanya sebentar, pada umumnya ikatan yang terjadi antara enzim dengan sel atau organ bukanlah ikatan kovalen akan tetapi ikatan hidrogen, ikatan ionik serta daya tarik antara gugus hidrofobik dari dua molekul itu sendiri yang bekerja secara bersama – sama mengikat substrat enzim, kebanyakan dari interaksi ini bersifat lemah terutama jika atom-atom yang bersangkutan berada di dalam jarak yang dekat oleh karena itu kedua molekul harus sangat berdekatan dan meliputi suatu area yang cukup luas agar suatu substrat enzim yang lemah dapat bereaksi sebagai katalisator protein.
Aktifitas enzim sangat dipengaruhi oleh keadaan suhu dan pH, tiap – tiap enzim dapat bekerja dengan efektif pada suhu dan pH tertentu dan aktivitasnya akan berkurang apabila dibawah atau diatas suhu serta pH rata – rata enzim untuk mengaktifasikan energy.
Sebagian enzim bekerja dalam suasana asam dimana indicator pH 1 s/d 2 dan sebagian enzim lainnya hanya mampu bekerja dalam suasana basa dimana rentan pH 8. Lemahnya kinerja kerja enzim dipengaruhi pula oleh bentuk ikatan yang terjadi secara kimiawi didalam tubuh serta structural tersier yang terbentuk didalam fungsi enzim. Enzim hanya mampu bekerja optimum pada suhu 38oC – 40oC dan pH antara 6-8, selain itu juga penambahan konsentrasi enzim dan konsentrasi substrat mengakibatkan kecepatan reaksi meningkat hingga dicapai kecepatan konstan. Adanya zat kimia tertentu juga dapat mempengaruhi kinerja kerja enzim sementara itu dengan adanya inhibitor enzim tidak dapat berikatan dengan substrat sehingga tidak dapat menghasilkan suatu produk.
Dalam hal ini terdapat dua macam inhibitor enzim yaitu inhibitor kompetitif dan inhibitor nonkompetitif. Inhibitor kompetitif adalah molekul penghambat yang cara kerjanya bersaing mendapatkan substrat sedangkan inhibitor nonkompetitif adalah molekul penghambat enzim yang bekerja dengan cara melekatkan diri pada luar sisi aktif sehingga bentuk enzim berubah dan sisi aktif tidak dapat berfungsi.
Aktifitas enzim di dalam sel diatur dengan ketat oleh kebutuhan tubuh dan aktifitas enzim pada substrat dapat diatur oleh molekul lain yang terikat pada tempat lain (allosterik) pada molekul enzim.
C. Ciri – ciri Enzim
Enzim memiliki ciri – ciri antara lain sebagai berikut :
- Enzim terdiri dari dua bagian yaitu :
- a) Apoenzim adalah bagian protein dari enzim yang tidak tahan akan panas dan berfungsi menentukan kekhususan pada enzim.
- b) Koenzim disebut sebagai gugus prostetik apabila terikat sangat erat pada apoenzim Akan tetapi, koenzim tidak begitu erat dan mudah dipisahkan dari apoenzim. Koenzim bersifat termostabil (tahan panas), mengandung ribose dan fosfat dimana . Fungsinya menentukan sifat dari reaksinya
- Enzim dapat mempercepat reaksi kimia akan tetapi tidak ikut bereaksi ( katalisator ).
- Enzim bekerja secara spesifik yaitu enzim tidak dapat bekerja pada semua substrat akan tetapi hanya bekerja pda substrat tertentu saja.
- Enzim berupa koloid dalam suatu larutan yang berfungsi sebagai pengaktifasi energy.
- Enzim dapat bereaksi pada substrat asam dan basa dikarenakan enzim mempunyai gugusresidu asam amino spesifik.
- Termolabil yang berarti apabila bekerja pada suhu rendah maka aktivitas enzim akan lambat dan jika bekerja pada suhu tinggi reaksi enzim akan semakin cepat, jika suhu terlalu tinggi maka enzim akan mengalami denaturasi.
- Kerja enzim bersifat bolak – balik (reversible) yaitu enzim tidak dapat menentukan arah reaksi akan tetapi hanya mempercepat laju reaksi hingga mencapai kesetimbangan.
Contoh – contoh enzim dalam proses metabolisme antara lain
- Enzim Katalase
Enzim katalase berfungsi membantu pengubahan hidrogen peroksida menjadi air dan oksigen.
- Enzim Oksidase
Enzim oksidase berfungsi mempercepat penggabungan O2 dengan suatu substrat yang pada saat bersamaan juga mereduksi O2, sehingga terbentuk H2O.
- Enzim Hidrase
Enzim Hidrase berfungsi menambah tau mengurangi air dari suatu senyawa tanpa menyebabkan terurainya senyawa yang bersangkutan. Contoh : fumarase, enolase, akonitase.
- Enzim Dehidrogenase
Enzim dehidrogenase berfungsi memindahkan hidrogen dari suatu zat ke zat yang lain.
- Enzim Transphosforilase
Enzim transphosforilase yaitu reaksi pemindahan suatu radikal bebas yang berfungsi memindahkan H3PO4 dari molekul satu ke molekul lain dengan bantuan ion Mg2+.
- Enzim Karboksilase
Enzim Karboksilase berfungsi dalam pengubahan asam organik secara bolak – balik yaitu reaksi pelepasan CO2 dan gugusan karboksil (–COOH). Contoh : pengubahan asam piruvat menjadi asetaldehide dibantu oleh karboksilase piruvat.
- Enzim Desmolase
Enzim desmolase berfungsi membantu dalam pemindahan atau penggabungan ikatan karbon. Contoh : aldolase dalam pemecahan fruktosa menjadi gliserildehida dan dehidroksiaseton.
- Enzim Peroksida
Enzim peroksida berfungsi membantu mengoksidasi senyawa fenolat, sedangkan oksigen yang diperlukan di ambil dari H2O2.
- Enzim Polimerase
Enzim polimerase berfungsi dalam memepercepat reaksi kimia dalam pembentukkan rantai nukleotida RNA yang lebih panjang serta pembentukkan RNA dengan penambahan dua gugus fosfat yang mempunyai ikatan berenergi tinggi.
Cara kerja enzim polimerase yaitu:
Enzim RNA polimerase akan menempel pada suatu tempat yang disebut promotor pada DNA. Kemudian enzim ini akan melepaskan untaian ganda DNA kedalam bentuk tunggal.
Enzim RNA polimerase membentuk nukleotida RNA sebagai komplemen dari DNA rantai tunggal tadi, setiap nukleotida RNA akan menggabung membentuk molekul RNA dengan menghubungkan fosfat dengan gula pada nukleotida lain melalui ikatan kovalen dan bantuan energy dari pelepasan dua gugus fosfat terakhir yang mempunyai ikatan berenergi tinggi. Kemudian Pada suatu tempat dalam DNA yang dinamakan chain terminating sequence enzim ini akan melepaskan diri.
Tidak lama setelah itu RNA akan terlepas dari DNA karena afinitas ikatan hidrogen antara DNA dengan DNA lebih besar daripada DNA dengan RNA.
Berikut tabel mengenai macam – macam enzim serta fungsinya :
|
NO |
Golongan Enzim |
Jenis Enzim |
Peranan Enzim |
|
1 |
Karbohidrase |
|
Menguraikan selulosa (polisakarida) menjadi selabiosa (disakarida)
Menguraikan amilum (polisakarida) menjadi maltosa (disakarida) Menguraikan pektin menjadi asam pectin Menguraikan maltosa menjadi glukosa Mengubah sukrosa menjadi glukosa dan fruktosa Mengubah laktosa menjadi glukosa dan galaktosa |
|
2 |
Protease | a. Pepsin
b. Tripsin c. Entrokinase d. Peptidase e. Renin f. gelatinase |
Memecah protein menjadi pepton
Menguraikanpepton menjadi asam aminoMenguraikan pepton menjadi asam amino Menguraikan peptida menjadi asam amino Menguraikan kasein dan susu Menguraikan gelatin |
|
3 |
Esterase | a. Lipase
b. Fostatase |
Menguraikan lemak menjadi gliserol dan asam lemak
Menguraikan suatu ester hingga terlepas asam fosfornya |
IKATAN KIMIA
IKATAN KIMIA
Ikatan Kimia
Ikatan kimia adalah sebuah proses fisika yang bertanggung jawab dalam interaksi gaya tarik menarik antara dua atom atau molekul yang menyebabkan suatu senyawa diatomik atau poliatomik menjadi stabil. Dengan kata lain ikatan kimia adalah kemampuan suatu atom bergabung dengan atom lain membentuk suatu senyawa.
Ikatan kimia dilakukan dengan melepas atau menerima electron, sehingga susunan electron menjadi stabil (seperti susunan pada gas mulia)
Kecenderungan unsur – unsur untuk menjadikan konfigurasi elektronnya sama seperti gas mulia terdekat dengan istilah aturan oktet
Elektron yang berperan dalam pembentukkan ikatan kimia adalah electron valensi dari suatu atom / unsur yg terlibat.
Ikatan kimia dapat dibedakan menjadi tiga macam yaitu ikatan ionik , ikatan kovalen dan ikatan kovalen koordinasi
1. Ikatan ion
Ikatan ion merupakan sejenis interaksi elektrostatik antara dua atom yang memiliki perbedaan elektronegatifitas yang besar
Ikatan ion terjadi apabila :
– Ikatan antara unsur logam dan bukan unsur logam
– Terjadi jika atom unsur yang memiliki energi ionisasi kecil / rendah melepaskan elektron valensinya (membentuk kation) dan atom unsur lain yang mempunyai afinitas elektron besar menangkap elektron tersebut (membentuk anion)
– Unsur logam melepaskan elektron sedangkan unsur non logam menerima elektron
Contoh : Ikatan ion yang membentuk senyawa KCl
KCl
19K : 2.8.8.1 17Cl : 2.8.7
Perhatikan jumlah elektron terluar pada susunan elektron dari kedua unsur diatas.
K akan melepaskan 1 elektron valensi
K ————-> K+
Cl menangkap 1 elektron valensi.
Cl ————> Cl–
Dengan begitu didapat susunan elektron dari kedua elektron yang stabil ( elektron kulit terluarnya berjumlah 8).
Pembentukan senyawa ionik sebagian berupa Siklus Born – Haber
a) Siklus Born – Haber
Pada pembentukkan senyawa ionik NaCl (s) dari Na ( s) dan Cl2 (s) diatas melibatkan serangkaian proses yang dinamakan dengan siklus Born-Haber
Entalpi kisi ( ∆Hkisi) merupakan perubahan entalppi standar yang menyertai pembentukan ion – ion gas dari padatan Kristal :
MX (s) ———> M+ (g) + X– (g) = ∆Hkisi
Semua entalpi kisi bernilai positif . Entalpi kisi berasal dari konstribusi energy elektrostatik total kation dan anion yang ada pada padatan ionik.
Contoh Soal :
Tentukan silus Born-Haber dan kalor pembentukkan LiF bila diketahui :
Kalor penguapan Li (s) = + 155 kJ/mol
Kalor disosiasi F2 (g) = + 158 kJ/mol
Energi kisi LiF (s) = – 1.016 kJ/mol
Energi ionisasi K (g) = +520 kJ/mol
Afinitas elektron (g) = – 328 kJ/mol
Solusi
Li(e) + ½F2 (g) ——> ∆H ——-> LiF (g)
F (g) ——> A ——-> F–
Li ( g) ——-> I ———–> Li+(g)
∆Hfo = S + I +½D + A + U
= ( 155 + 520 + 79 – 328 – 1016 ) kJ
= – 590 kJ/mol
2. Ikatan Kovalen
Ikatan kovalen adalah ikatan yang terjadi jika ada pemakaian pasangan elektron secara bersama- sama oleh atom-atom yang berikatan, dikarenakan ketidak mampuan salah satu atom yang akan berikatan untuk melepaskan elektron ( terjadi pada atom – atom non logam).
Sifat – sifat atom yang membentuk ikatan kovalen sebagai berikut :
· Terbentuk diantara dua atom yang sama-sama ingin menangkap elektron
· Sesudah berikatan tiap atom harus dikelilingi 2 atau 8 elektron
· Atom-atom yang memiliki afinitas elektron tinggi serta beda keelektronegatifannya lebih kecil dibandingkan ikatan ion.
Ikatan kovalen terbagi atas dua macam berdasarkan kepolarannya antara lain :
a) Ikatan Kovalen Polar
Ikatan kovalen polar terjadi jika pasangan elektronnya yang dipakai bersama-sama, tertarik lebih kuat ke salah satu atom yang berikatan (berdasarkan atas keelektronegatifan unsurnya berbeda).
Elektron akan tertarik lebih kuat ke atom yang elektronegatif lebih besar (cenderung menangkap elektron)
Contoh :
b) Ikatan Kovalen Non Polar
Ikatan kovalen non polar terjadi jika pasangan elektron yang dipakai bersama, sama kuat ke semua atom yang berikatan. Ikatan ini terjadi dengan syarat dua atom yang berikatan mempunyai keelektronegativitas yang sama.
Pada molekul yang simetris seperti CaCl2, BaCl2 , AlCl3 dan CCl4 polaritas masing – masing ikatan akan saling meniadakan sehingga molekul tersebut bersifat non polar.
Contoh :
3. Ikatan Kovalen Koordinasi
Ikatan kovalen koordinasi adalah ikatan kovalen dengan pasangan elektron yang digunakan secara bersama hanya berasal / disumbangkan oleh salah satu atom
Berikut Tabel perbedaan antara ikatan ionik , kovalen dan kovalen koordinasi
|
Perbedaan |
Ionik |
Kovalen |
Kovalen Koordinasi |
| Proses Pembentukkan | Serah terima elektron antar atom | Penggunaan bersama pasangan elektron dimana tiap atom menyumbang elektron
X. + .Y à X:Y |
Penggunaan bersama pasangan elektron yang hanya berasal dari salah satu atom
X: + Y à X:Y |
| Atom yang terlibat | Logam + Nonlogam | Nonlogam + Nonlogam | Nonlogam + Nonlogam |
| Titik leleh & Titik Didih | Tinggi | Rendah ( kecuali pada padatan kovalen seperti intan ) | Rendah |
| Kealrutan | Larut dalam air namun sukar larut dalam pelarut organik seperti aseton, alcohol,eter dan Benzena | Sukar larut dalam air namun larut dalam pelarut organik | Sukar larut dalam air namun larut dalam pelarut organic |
| Daya Hantar Listrik | Lelehan dan larutannya menghantarkan listrik | Tidak dapat menghantarkan listrik (namun ada beberapa larutannya yg menghantarkan listrik) | Tidak dapat menghantarkan listrik (namun ada beberapa larutannya yg menghantarkan listrik) |
| Contoh | NaCl , LiF, CaO, CaBr2 , AlCl3 | HF, H2O, PCl3 , BCl3 , CO2 | NH4+ , SO4-2 , POCl3, H3NBF3 , SO3 |
Kesimpulannya Kepolaran suatu senyawa dipengaruhi oleh adanya perbedaan keelektronegatifan antara atom – atom yang berikatan dan bentuk molekul. Suatu senyawa akan dikatakan polar apabila selisih keelektronegatifan antara atom penyusunnya semakin besar. Selain itu ketidaksimetrisan bentuk molekul juga menyebabkan senyawa bersifat polar. Adanya muatan elektron yang tidak seimbang antar atom dalam senyawa polar mengakibatkan terjadinya suatu kutub (dipol). Oleh karena itu, pasangan elektron yang digunakan untuk membentuk ikatan kovalen polar lebih kuat tertarik pada salah satu atom.
Sebaliknya suatu senyawa dikatakan bersifat nonpolar jika terbentuk dari atom sejenis atau senyawa yang distribusi muatannya simetris contoh H2 atau CH4. Harga elektronegatifitas atom – atom dalam molekul nonpolar sama, sehingga muatan elektronnya terdistribusi secara merata. Oleh karena itu molekul nonpolar tidak membentuk kutub. Pasangan elektron senyawa nonpolar mengakibatkan bentuk molekul simetris sehingga dipol – dipol ikatannya saling meniadakan.
4. Ikatan Hidrogen
Ikatan Hidrogen adalah ikatan yang terbentuk karena adanya gaya tarik menarik atom yang elektronegatifitasnya sangat besar, ikatan ini merupakan ikatan antar molekul yang sangat polar, ikatan ini lebih kuat daripada ikatan van der walls dan mempunyai arah yang jelas seperti atom F,O, dan N terhadap atom H. Contohnya : NH3 , H2O dan HF
Dengan adanya ikatan hidrogen menyebabkan terjadinya keadaan sebagai berikut :
· Air mempunyai Mr kecil akan tetapi mempunyai titik didih yang tinggi ( setiap senyawa yang mempunyai ikatan hidrogen mempunyai titik didih yang tinggi ).
· Molekul air lebih berdekatan ( jarak antara molekul ) dibandingkan molekul es (padat), yang akan mengakibatkan es mengapung di atas air.
Ikatan Hidrogen merupakan ikatan antar molekul yang sangat polar dan mengandung atom hidrogen. Dalam keadaan cair atom hidrogen dalam molekul air yang parsial positif (δ+) ditarik oleh pasangan elektron atom O molekul lain yang elektronegatif, sehingga terbentuk ikatan hidrogen.
Ikatan Hidrogen jauh lebih kuat daripada gaya-gaya van der walls. Zat yang mempunyai ikatan hidrogen memerlukan energy yang besar untuk memutuskannya. Oleh karena itu titik didih dan titik lelehnya sangat tinggi.
5. Ikatan Van der Walls
Ikatan van der walls adalah gaya tarik menarik antarmolekul (antar kutub) dalam senyawa yang berikatan kovalen. Gaya ini merupakan gaya antarmolekul yang sangat lemah Mencakup interaksi dipole – dipole (pada senyawa polar) dan interaksi dipole terimbas/terinduksi (pada senyawa polar dan non polar). Sedangkan interaksi dipole sementara (pada senyawa non polar) biasa disebut dengan gaya dispersi London.
Semakin besar Mr suatu senyawa (semakin banyak jumlah partikel yang saling tarik) ikatan van der walls akan semakin kuat, sehingga energy yang dibutuhkan untuk memutuskan ikatan antarmolekul semakin besar. Akibatnya titik leleh dan titik didih senyawa tersebut akan semakin besar.
Pada ikatan Van der walls dibagi menjadi 2 bagian yaitu gaya London dan gaya tarik dipol
- Gaya London
Gaya London ditemukan oleh Fisikawan Jerman yang bernama Fritz London. Gaya London (gaya dispersi) merupakan gaya tarik menarik antar molekul nonpolar akibat adanya dipol terimbas yang ditimbulkan oleh perpindahan elektron dari satu orbital ke orbital lain membentuk dipol sesaat. Gaya London mengakibatkan molekul nonpolar bersifat agak polar.
Kemudahan suatu molekul menghasilkan dipol sesaat yang dapat mengimbas ke molekul sekitarnya disebut polarisabilitas. Polariabilitas berkaitan dengan massa molekul relatif (Mr) dan bentuk molekul. Jika massa molekul relatif semakin besar maka molekul semakin mudah mengalami polarisasi sehingga gaya London semakin kuat. Dengan massa molekul relatif yang sama besar molekul yang bentuknya panjang lebih mudah mengalami polarisasi dibandingkan dengan molekul yang kecil, kompak dan simetris. Semakin mudah mudah molekul mengalami polarisasi semakin tinggi titik didih dan titik lelehnya. Oleh karena itu jika masa molekul relatif zat semakin besar maka titik didih dan titik lelehnya semakin tinggi.
Namun gaya London relatif lemah sehingga apabila suatu zat yang molekulnya hanya mengalami tarik menarik berdasarkan gaya London saja maka titik didih dan titik lelehnya lebih rendah dibandingkan zat lain yang mengalami tarik-menarik tidak hanya berdasarkan gaya London saja (Mr hampir sama).
- Gaya Tarik Dipol
Gaya Tarik Dipol adalah suatu molekul – molekul polar yang cenderung menyusun diri dengan cara saling mendekati kutub positif dari suatu molekul dengan kutub negatif molekul yang lain.
Semakin besar momen dipol yang dimiliki oleh suatu senyawa, semakin besar gaya tarik menarik dipol yang dihasilkan. Gaya ini lebih kuat dibandingkan dengan gaya London. Oleh karena itu, molekul yang mengalami gaya tarik dipol memiliki titik didih dan titik leleh yang lebih tinggi daripada molekul yang mengalami gaya London (Mr hampir sama).
Gaya Tarik dipol terdiri atas 5 jenis yang berbeda antara lain :
- Gaya Dipol – Dipol
Gaya ini akan terjadi jika sesama senyawa kovalen polar saling berinteraksi. Senyawa kovalen polar memiliki 2 dipol yaitu dipol positif (δ+) dan dipol negatif (δ–). Interaksi antara dipol (-) dari satu molekul dengan dipol (+) dari satu molekul yang lain akan menimbulkan gaya tarik yang relatif lemah.
Kekuatan gaya tarik dipol – dipol ini akan semakin besar jika molekul – molekul mengalami penataan dengan ujung (+) suatu molekul mengarah keujung (-) dari molekul yang lain.
- Gaya Dipol Sesaat.
Jenis gaya ini umumnya dimiliki oleh senyawa kovalen nonpolar. Berbeda dengan senyawa kovalen polar, senyawa kovalen nonpolar tidak memiliki dipole. Gaya ini terjadi akibat adanya pergerakan elektron mengelilingi inti atom secara acak, sehingga pada suatu saat elektron – elektron tersebut akan mengumpul pada salah satu sisi atom dari molekul. Dipol yang terjadi ini akan segera menghilang atau berpindah tempat (sisi) seiring dengan berputarnya elektron.
- Gaya Dipol – Dipol Terinduksi (gaya imbas)
Jika suatu molekul polar berdekatan dengan molekul nonpolar maka molekul polar dapat menginduksi molekul nonpolar, akibatnya molekul nonpolar tersebut akan memiliki dipol terinduksi / dipol sesaat karena elektron – elektronnya akan mengumpul pada salah satu sisi molekul ( terdorong atau tertaik ).
Gaya dipol – dipol terinduksi (gaya imbas) adalah suatu dipol dari molekul polar akan saling tarik menarik dengan dipol terinduksi dari molekul nonpolar.
- Gaya Ion – Dipol
Gaya jenis ini terjadi antara senyawa ion dan senyawa kovalen polar. Ketika dilarutkan dalam senyawa kovalen polar, senyawa ion ini akan terionisasi menjadi kation dan anion. Kation akan tarik-menarik dengan dipol negatif sedangkan anion akan tarik-menarik dengan dipol positif.
- Gaya Ion – Dipol Sesaat
Mekanisme terjadinya gaya ini dikarenakan kombinasi dari proses terjadinya gaya dipol – dipol terinduksi dengan gaya ion – dipole. Jika ion dari senyawa ion berdekatan dengan molekul nonpolar maka ion tersebut dapat menginduksi dipol molekul nonpolar. Dipol terinduksi molekul nonpolar yang dihasilkan akan berikatan dengan ion.
Jenis gaya seperti ini memegang peranan penting dalam sirkulasi darah di dalam tubuh. Ion Fe2+ dalam haemaglobin akan mengalami gaya ion – dipol sesaat dengan molekul O2. Kation Fe2+ akan menginduksi molekul O2 yang bersifat nonpolar, kemudian dipol terinduksi yang dihasilkan akan berikatan dengan kation Fe2+.
6. Ikatan Logam
Ikatan Logam adalah ikatan yang terbentuk karena elektron-elektron pada logam dapat bergerak bebas membentuk awan elektron yang mengikat logam-logam bermuatan positif. Awan elektron yang dapat bergerak bebas ini dapat menghantarkan arus listrik.
Atom logam mempunyai sedikit valensi sehingga sangat mudah untuk dilepaskan dan membentuk ion positif, dikarenakan kulit terluar atom logam relatif longgar (terdapat banyak ruang kosong) sehingga memungkinkan elektron dapat berpindah dari satu atom ke atom yang lain.
Mobilitas (pergerakan) elektron dalam logam sedemikian bebas sehingga elektron valensi logam mengalami delokalisasi yaitu suatu keadaan dimana elektron valensi tersebut tidak tetap pada posisinya akan tetapi senantiasa berpindah – pindah dari satu atom ke atom lainnya.
Gambar Ikatan Logam yang terbentuk.
7. Ikatan Valensi
Ikatan valensi yaitu ikatan yang terbentuk melalui tumpang tindih (overlap) orbital valensi antara atom satu dengan atom lainnya. Orbital yang mengalami overlap harus memiliki hanya satu elektron dengan spin yang berlawanan. Overlapping terjadi apabila orientasi ( bentuk) orbital sesuai.
Overlapping orbital p dapat terjadi dalam dua orientasi yang berbeda yaitu overlapiing muka-muka dan badan-badan. Overlapping antar muka menghasilkan ikatan σ dan overlapping antar badan menghasilkan ikatan ∏.